
Het immuunsysteem en chronische pijn: waarom pijn blijft als de schade weg is
Stel je voor: je verzwikt je enkel. Auw, een minder moment in het leven. Het zwelt op, wordt blauw, Je loopt een paar dagen wat moeizaam, en dan - langzaam maar zeker - trekt het weg. Eerst de zwelling, dan de pijn, dan de stijfheid. Na een paar weken is het voorbij. Case closed. Volgende blessure. Zo werkt acute pijn.
Maar bij chronische pijn gebeurt dat niet. De pijn blijft. Niet een beetje. Of anders. Het blijft. Soms maanden. Soms jaren. En als je gaat kijken naar het weefsel - met scans, echo's, wat dan ook - zie je vaak: weinig. De oorspronkelijke schade is geheeld, of was er nooit in die mate.
Dat vertelt ons iets cruciaals: pijn is niet een betrouwbare maatstaf voor schade. Er speelt iets anders.
Het systeem dat zichzelf in stand houdt
Hier is wat we de afgelopen twee decennia hebben geleerd : chronische pijn ontstaat wanneer je immuunsysteem en je zenuwstelsel een telefoongesprek beginnen dat ze vergeten te beëindigen.
Normaal gesproken werkt het zo: weefsel raakt beschadigd, immuuncellen komen kijken, ze ruimen de boel op, zenuwen vertellen je hersenen "dit doet pijn, wees voorzichtig", en dan - als het weefsel heelt - houdt het gesprek op. Men hangt op, iedereen gaat weer andere dingen doen.
Bij chronische pijn blijven ze praten. Het immuunsysteem blijft signalen sturen naar de zenuwen, de zenuwen blijven signalen sturen naar het ruggenmerg en de hersenen, en die sturen weer signalen terug naar het immuunsysteem. Een feedbackloop. En die loop - dat is waar pijn zijn kans krijgt om chronisch te worden.

Laten we kijken hoe dat in zijn werk gaat. Want het is niet vaag of mysterieus. Het is al vrij goed begrepen.
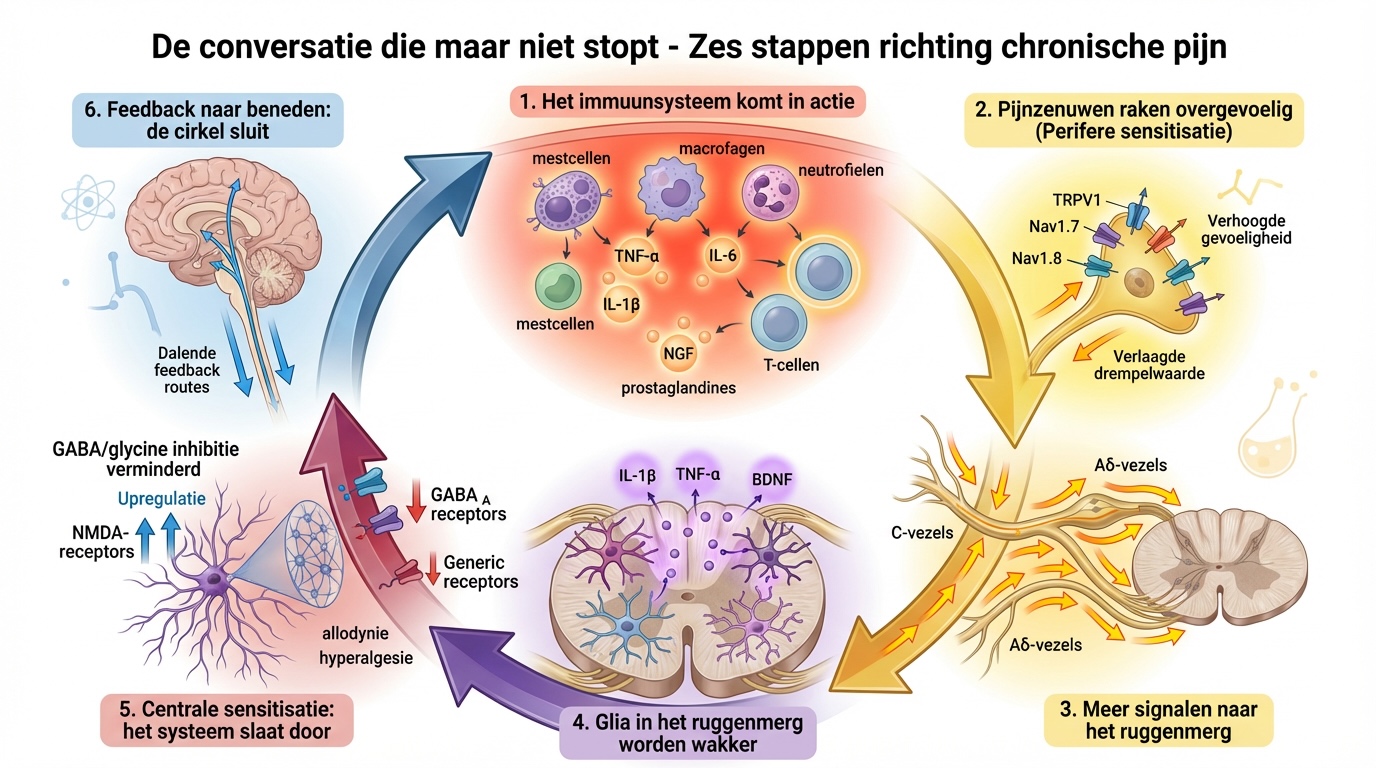
De conversatie die niet stopt: zes stappen die elkaar voeden
Stap 1 : Immuuncellen komen in actie
Stap 2: Zenuwen worden prikkelbaarder
Stap 3: Meer signalen naar het ruggenmerg
Stap 4: Gliacellen in het ruggenmerg worden wakker
Stap 5: Het centrale zenuwstelsel wordt gevoeliger
Stap 6: Deze signalen worden weer stimulerend teruggekoppeld naar de plek van oorsprong
Stap 1: Immuuncellen komen in actie
Ergens in je lichaam - laten we zeggen een gewricht dat artrotisch is, of een zenuw die geïrriteerd raakt, of spierweefsel dat overbelast is - komen immuuncellen in actie. Mestcellen, macrofagen, neutrofielen, T-cellen. Ze doen wat ze geacht worden te doen: opruimen, beschermen, signaleren.
Ze doen hun werk geven stoffen af. TNF-α, interleukines (IL-1β, IL-6), prostaglandinen, nerve growth factor (NGF). Dat zijn geen vage "ontstekingsmediatoren" - het zijn specifieke moleculen met concrete effecten.
En één van die effecten is: ze maken de uiteinden van zenuwen gevoeliger.
Stap 2: Nociceptoren worden prikkelbaarder
Stel je een zenuw voor , of preciezer en beter: de nociceptor, het uiteinde van die zenuw dat schadelijke prikkels detecteert. Normaal gesproken reageert zo'n nociceptor op sterke prikkels: druk, hitte, chemische irritatie. Er is een drempelhoogte voor doorgeven van het signaal. Onder die drempel: geen signaal. Boven die drempel: signaal naar je ruggenmerg en hersenen.
Maar die ontstekingsmediatoren van je immuuncellen die we bij stap 1 zagen doen iets slims: ze maken de ionkanalen in die nociceptor gevoeliger.
TRPV1, Nav1.7, Nav1.8 - dat zijn de kanaaltjes die opengaan en een elektrisch signaal starten.
Door die mediatoren gaat de drempel omlaag. Prikkels die normaal niks doen, triggeren nu wél een signaal. Soms vuren nociceptoren spontaan, zonder dat er überhaupt een prikkel is.
Dat heet perifere sensitisatie. Het zenuwuiteinde is nu overgevoelig.
Stap 3: Verhoogde signalen naar het ruggenmerg
Logisch gevolg: als je nociceptoren gevoeliger zijn, sturen ze meer signalen. Hogere frequentie, meer intensiteit. Die signalen reizen via C-vezels en Aδ-vezels (de langzame en snelle pijnbanen) naar het ruggenmerg.
Tot zover is dit nog relatief normaal. Meer input betekent meer signaal. Maar hier begint het interessant te worden.
Stap 4: Glia in het ruggenmerg worden wakker
In je ruggenmerg - specifiek in de dorsale hoorn, het deel waar pijnsignalen binnenkomen - zitten cellen die we nog niet zo lang geleden beschouwden als alleen "ondersteunend": de microglia en astrocyten. Gliacellen. We dachten dat ze structuur boden, voedingsstoffen doorgaven, afval opruimden. Passief werk.
Maar we leerden: ze zijn niet passief. Ze luisteren mee. En ze hebben ook nog een mening over wat ze horen.
Wanneer neuronen in de dorsale hoorn voortdurend geactiveerd worden door die verhoogde input, geven ze stoffen af - ATP, fractalkine - die de gliacellen activeren. En die gliacellen, die schakelen over naar een pro-inflammatoir profiel en beginnen zélf mediatoren af te geven: IL-1β, TNF-α, brain-derived neurotrophic factor (BDNF).
En die stoffen doen op hun beurt iets heel specifieks: ze maken de synapsen tussen neuronen prikkelbaarder.
Stap 5: Centrale sensitisatie - het systeem draait op toeren
Dit is waar het systeem echt van koers raakt.
Door die gliale mediatoren worden pijnbanen in je ruggenmerg en hersenen versterkt:
NMDA-receptoren worden upgereguleerd (meer receptoren = meer signaal)
Inhibitie neemt af (GABA en glycine, de "remmers", werken minder goed)
Er ontstaan LTP-achtige mechanismen - dat wil zeggen Long-Term Potentiation, hetzelfde proces dat bij geheugenvorming hoort, maar nu in pijnbanen
Receptieve velden breiden uit: neuronen die normaal alleen reageren op input van je pink reageren nu ook op input van je ringvinger
Het resultaat: pijnsignalen worden harder doorgegeven dan ze zouden moeten. Lichte aanraking voelt pijnlijk (allodynie). Pijnlijke prikkels voelen extreem pijnlijk (hyperalgesie). Pijn verspreidt zich naar gebieden die niet beschadigd zijn.
Dat is centrale sensitisatie. Je pijnsysteem is overgevoelig geworden, niet alleen in de periferie, maar in het centrale zenuwstelsel zelf.
Stap 6: Feedback naar beneden - descendente facilitatie
En hier sluit de cirkel zich. Die verhoogde activiteit in hersenen en ruggenmerg stuurt signalen terug naar beneden - descendente banen die normaal pijn moduleren. Maar in plaats van te dempen, faciliteren ze. Ze houden het perifere immuunsysteem actief, ze houden nociceptoren gevoelig.
En zo draait de cyclus door. Immuuncellen → gevoelige nociceptoren → verhoogde input → gliale activatie → centrale sensitisatie → feedback naar periferie → immuuncellen blijven actief.
De oorspronkelijke trigger - de verstuikte enkel, de artrose, de zenuwirritatie - is niet meer nodig. Het systeem voedt zichzelf.
Dat is waarom pijn blijft als de schade weg is.
Maar waarom gebeurt dit niet bij iedereen?
Goede vraag. Als dit mechanisme zo universeel is, waarom wordt pijn dan niet bij iedereen chronisch na een blessure? Omdat er kwetsbaarheidsfactoren zijn. Dingen die bepalen of die feedbackloop blijft draaien of uitdooft.
Een blijvende perifere prikkel
Als er iets is dat het immuunsysteem blijft activeren - artrose die niet weggaat, een zenuw die mechanisch geïrriteerd blijft, endometriose - dan blijft die eerste stap actief. De loop krijgt brandstof.
Stress en slaap
Je HPA-as (hypothalamus-hypofyse-bijnier - het systeem dat stress reguleert) en je slaap beïnvloeden je immuunsysteem. Chronische stress en slaaptekort geven een pro-inflammatoire bias. Je immuunsysteem staat meer "aan" dan het zou moeten. Dat maakt die feedbackloop gemakkelijker om te starten en moeilijker om te stoppen.
(Epi)genetische verschillen
Sommige mensen hebben genetische varianten die hun immuunsysteem reactiever maken. Niet goed of slecht, gewoon anders. Dat kan het verschil maken tussen pijn die overgaat en pijn die blijft.
Sekse-afhankelijke verschillen
In diermodellen zijn er duidelijke verschillen in hoe glia en immuuncellen reageren tussen mannelijke en vrouwelijke dieren. Bij mensen is het bewijs complexer (zoals altijd met translatie van diermodel naar mens), maar het patroon lijkt er te zijn. Vrouwen hebben vaker chronische pijn dan mannen, en mechanistisch lijkt er verschil te zitten in hoe glia reageren.
Het gaat dus niet om één oorzaak. Het is een samenspel van hoeveel input het systeem krijgt en hoe dat specifieke systeem daarop reageert.
En wat betekent dit voor behandeling?
Als je dit mechanisme begrijpt, ga je anders kijken naar therapieën. Niet "wat helpt tegen pijn in het algemeen", maar "welke schakel in dit systeem kun je beïnvloeden, en bij wie?"
Therapie werkt het best als je het mechanisme matcht met het pijntype - logisch, maar verrassend vaak niet toegepast.
Gericht op specifieke schakels:
Anti-NGF bij artrose
Weet je nog, nerve growth factor? Die stof die immuuncellen afgeven en die nociceptoren gevoeliger maakt? Als je die blokkeert met antistoffen (zoals tanezumab), zie je pijnreductie bij mensen met artrose.
Het werkt. Maar er zijn veiligheidsproblemen - gewrichtsgerelateerde bijwerkingen, waarschijnlijk omdat NGF ook een rol speelt in weefselonderhoud. Dat heeft de toepassing beperkt.
Praktisch: relevant bij artrosepijn die niet reageert op standaardbehandeling, maar geen wondermiddel.
Glia-modulatie: Low-dose naltrexone bij fibromyalgie
Low-dose naltrexone (LDN) wordt vaak gezien als neuro-immuun/glia-modulator. Het idee: het dempt die pro-inflammatoire overstap van glia zonder het immuunsysteem compleet plat te leggen
Een recente gerandomiseerde, dubbelblinde, placebo-gecontroleerde studie in The Lancet Rheumatology (2024) onderzocht naltrexon 6 mg bij vrouwen met fibromyalgie - gerandomiseerd, dubbelblind, placebo-gecontroleerd, dus iedereen blij. Ze vonden significante effecten, maar de effectgrootte was bescheiden.
Praktisch: interessant bij wijdverspreide pijn zoals fibromyalgie. Werkt niet bij iedereen, en we weten nog niet goed hoe we de responders vooraf kunnen identificeren. Maar voor sommige mensen maakt het verschil. The proof is in the pudding..
Immunomodulatie bij selecte subgroepen: IVIG bij refractaire CRPS
Bij een deel van CRPS-patiënten (Complex Regional Pain Syndrome) lijkt een immuun- of auto-immuuncomponent mee te spelen. Een RCT in Annals of Internal Medicine (2010) rapporteerde pijnreductie met intraveneus immunoglobuline (IVIG) bij refractaire CRPS.
Praktisch: Dit is geen eerstelijnsbehandeling. Het past alleen bij zorgvuldige selectie in een specialistische setting. Denk: uitgeprobeerd wat redelijk is, niets helpt, er zijn aanwijzingen voor immuunbetrokkenheid. In Nederland zit een groot CRPS-centrum in het Erasmus.
Cytokineremming: TNF-α-remmers
TNF-α-remming (met biologicals zoals die gebruikt worden bij reumatoïde artritis) is onderzocht in verschillende pijncontexten. Resultaten zijn wisselend. Succes hangt sterk af van of er daadwerkelijk TNF-α-gedreven inflammatie is.
Praktisch: logisch bij duidelijke inflammatoire pathologie (reumatische aandoeningen, inflammatoire darmziekten). Veel minder effectief bij aspecifieke chronische pijn zonder aanwijzingen voor actieve ontsteking. En dat is logisch - als er geen TNF-α-proces is, ga je dat ook niet remmen.
De stille werkpaarden: 'immuunvriendelijke' basisinterventies

Hier wordt het leuk. Er zijn interventies die geen echte immunotherapie zijn, maar die wél je immuunsysteem (en je pijnsysteem) beïnvloeden. En ze werken. Wellicht niet spectaculair, en zo snel als we graag willen, maar consistent:
1. Graded activity en oefentherapie
Spieren produceren myokines - signaalstoffen - bij activiteit. Sommige daarvan zijn anti-inflammatoir. Beweging verbetert ook stressregulatie, wat indirect je immuunsysteem gunstig beïnvloedt.
Dit klinkt vaag, de effecten zijn meetbaar. Graded activity en oefentherapie zijn consistent effectief bij chronische pijn, en dit is één van de mechanismen waarom.
2. Slaapinterventies
Slaaptekort verhoogt pro-inflammatoire cytokinen. Die cytokinen maken je gevoeliger voor pijn. Die verhoogde pijngevoeligheid maakt slapen moeilijker. Het is een vicieuze cirkel, maar je kunt hem doorbreken.
Beter slapen → minder inflammatoire bias → minder pijngevoeligheid. Het is niet direct en niet spectaculair, maar het werkt.
3. Gewichts- en metabole gezondheid
Adipositas gaat samen met laaggradige inflammatie. Niet altijd, niet bij iedereen, maar vaak genoeg dat het relevant is. Overtollig vetweefsel - vooral visceraal vet - produceert ontstekingsmediatoren. Dezelfde mediatoren die we zagen in stap 1 van onze cyclus.
Metabole optimalisatie (gewichtsverlies waar dat relevant is, betere glucoseregulatie) vermindert die inflammatoire belasting. En dat helpt, niet alleen voor je algemene gezondheid, maar ook voor pijngevoeligheid.
4. Psychologische interventies
Cognitieve gedragstherapie, acceptance and commitment therapy, mindfulness - ze werken. Niet omdat pijn "tussen je oren zit" (dat zit het niet), maar omdat ze stress beïnvloeden, en stress beïnvloedt je immuunsysteem en je pijnnetwerken.
Daarnaast is er tegenwoordig nog een variant hierop: de EAET, en de PRT, gericht op het herstructureren van verwachtingen en het verwerken van emoties. Studies laten goede resultaten zien.
Het effect is indirect, maar reëel.
Deze interventies worden vaak gezien als "algemeen gezond" - wat ze ook zijn. Maar ze passen perfect in dit neuro-immuun-plaatje. Ze beïnvloeden de systemen die pijn in stand houden, zonder dat je er recepten voor nodig hebt of specialistische behandeling.
Wanneer denk je extra aan een immuuncomponent?
Dit is niet een diagnostisch algoritme. Het helpt als richtinggevend kader om te denken: past een immuuncomponent bij dit plaatje?
Denk eraan bij:
- Bekende inflammatoire aandoeningen: Reumatoïde artritis, inflammatoire darmziekten, psoriasis, spondyloartritis. Logisch - er is een inflammatoir proces, dus een neuro-immuun-interactie ligt voor de hand.
- CRPS met uitgesproken autonome of ontstekingsachtige kenmerken: Zwelling die niet past bij wat je verwacht, kleursverandering, temperatuurverschil. Dat suggereert dat er meer speelt dan alleen zenuwdysfunctie.
- Pijn met duidelijke post-infectieuze start: Begon na een infectie (Lyme, COVID, EBV, wat dan ook) en bleef daarna hangen. Het immuunsysteem was in hoge staat van paraatheid en is misschien niet goed afgeschakeld.
- Systemische klachten: Vermoeidheid die niet past, koorts, gewrichtspijn op meerdere plekken. Dat wijst op systemische immuunactivatie.
- Comorbiditeit met auto-immuunfenomenen of immuundeficiëntie Schildklierproblematiek, andere auto-immuunaandoeningen in de familie, laboratoriumafwijkingen die wijzen op immuundisregulatie.
- Laboratorium- of beeldvormingsbevindingen die inflammatie ondersteunen: Verhoogd CRP, verhoogde bezinking, actieve inflammatie op MRI. Altijd in context geïnterpreteerd, niet als op-zichzelf-staand bewijs
Het is geen checklist. Het is een manier om te denken: past dit patroon bij deze patiënt?
Samenvattend
Chronische pijn ontstaat wanneer je immuunsysteem en zenuwstelsel een gesprek beginnen dat ze vergeten te beëindigen:
Immuuncellen sensitiseren nociceptoren, die sturen meer signalen naar het ruggenmerg, glia daar worden geactiveerd, centrale sensitisatie ontstaat, en die centrale activiteit houdt het perifere immuunsysteem weer actief. Een feedbackloop die zichzelf voedt.
Daarom blijft pijn bestaan als de oorspronkelijke schade weg is. Het systeem heeft die trigger niet meer nodig.
Therapie werkt het best als je het mechanisme matcht met het pijntype - logisch, maar verrassend vaak niet toegepast:
Anti-NGF bij artrose (blokkeer de brug tussen inflammatie en zenuwsensitisatie)
LDN bij wijdverspreide pijn (moduleer gliale activiteit)
IVIG bij specifieke CRPS-subgroepen (immunomodulatie waar auto-immuniteit meespeelt)
Cytokineremming bij aantoonbare inflammatoire aandoeningen (richt je op het inflammatoire proces zelf)
Er is geen panacee, niet één wondermiddel. Het gaat om begrijpen welk systeem ontregeld is, en welke interventie daar het beste bij past.
En ja - beweging, slaap, gezond eten, en stressmanagement. Ze zijn niet spectaculair, wellicht niet sexy en instagrammable. Maar ze werken precies daar waar het systeem vastloopt. Het is laaghangend fruit.

