
"het hoofdpijn dossier"
Migraine
Migraine is geen gewone hoofdpijn.
Wie het heeft, weet dat. Wie het niet heeft, begrijpt het meestal niet - hoe goedbedoeld de reacties ook zijn.
"Heb je al paracetamol geprobeerd?” Of "Misschien moet je wat meer water drinken".
Het zijn de migraine-equivalenten van "Er zijn genoeg vissen in de zee" of "Kop op, het had erger gekund".
Wellicht vriendelijk bedoeld, en inhoudelijk misplaatst, en ver naast de werkelijkheid.
Migraine is geen doorsnee hoofdpijn, niet overdreven, niet het gevolg van te weinig water drinken, tenminste, niet in de manier waarop mensen dat doorgaans bedoelen. Het is een complexe neurologische aandoening. Een ontregeling van een overprikkelbaar brein.
Het is een aandoening waarbij je zenuwstelsel, je hersenvliezen, je bloedvaten en een reeks biochemische ketens samen een aanval produceren die zo invaliderend kan zijn dat mensen dagenlang in een verduisterde kamer liggen, niet in staat om te functioneren.
Omdat het licht te fel is. Omdat het geluid snijdt. Omdat er een misselijkheid is die alles overheerst. Omdat beweging alles verergert.
Dat verdient een uitleg die even serieus is als de aandoening zelf.
Deel 1: Hoe begint een migraineaanval?
De hersenen die te snel op scherp staan
Mensen met migraine hebben hersenen die, structureel gezien, gevoeliger zijn voor prikkels dan gemiddeld.
Op MRI-scans is te zien dat de hersenschors van migrainepatiënten vaker en heftiger reageert op lichtflitsen, geluiden en andere stimuli dan die van mensen zonder migraine
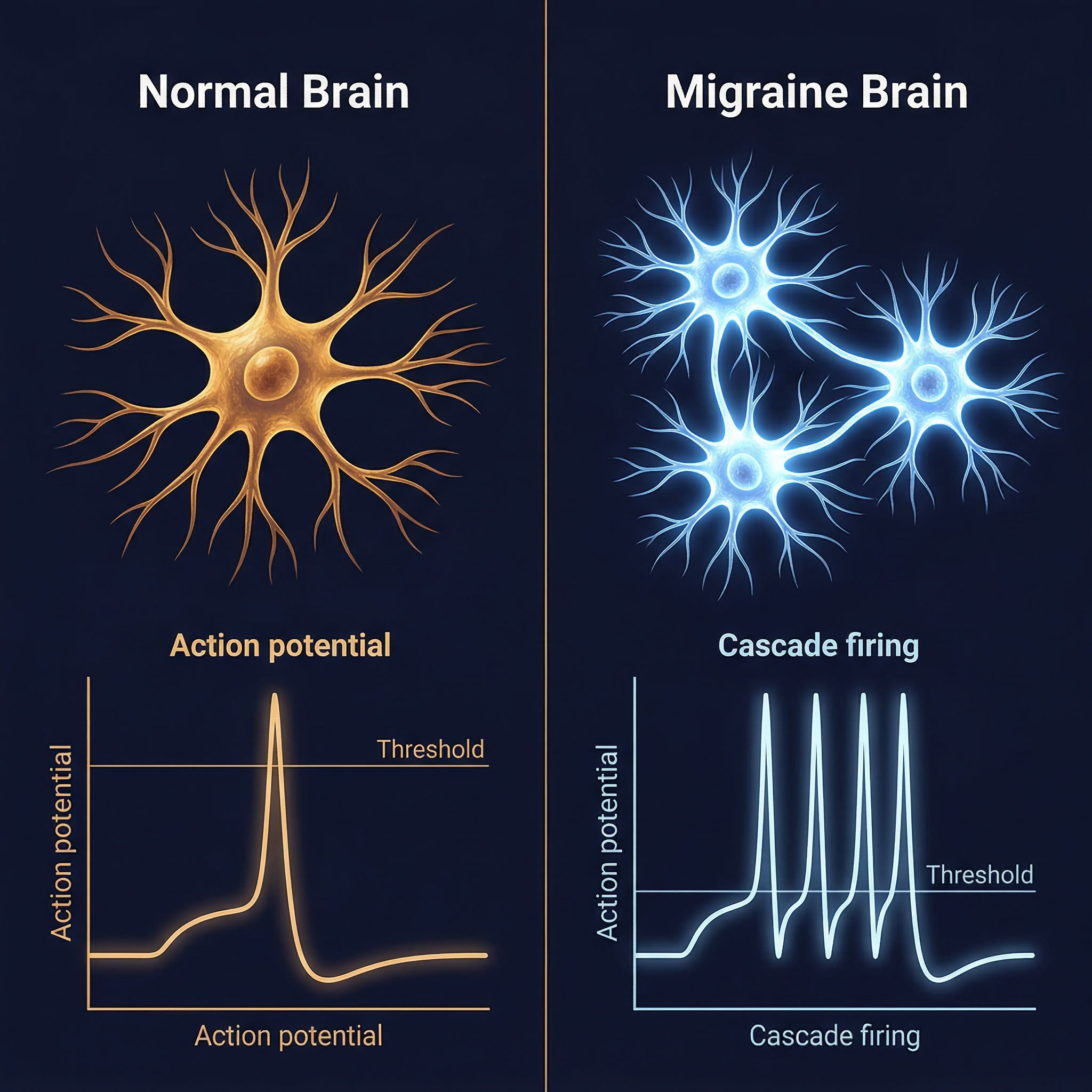
Dit noemen we verhoogde corticale excitabiliteit, de drempel waarop neuronen actief worden ligt lager, en als één neuron actief wordt, neemt het zijn buren gemakkelijker mee. Het geeft een cascadewerking door de verlaagde remmende tonus, en de verhoogde synaptische prikkelbaarheid.
Dit verklaart iets wat mensen met migraine vaak zelf ook al aanvoelen: dat hun aanvallen worden uitgelokt door dingen die bij anderen geen aanval veroorzaken. Felle lichten, bepaalde geuren, slaaptekort, hormonale schommelingen, stress, een glas rode wijn of toevoegingen in voedsel. Dit alles zijn voorbeelden en zijn geen tekenen van zwakte of overgevoeligheid als karaktereigenschap, het is biologie.
Het alarm staat scherper gecalibreerd, en er is minder nodig om het te laten afgaan
Uren voordat de pijn begint: de prodromale fase
Een migraineaanval begint niet met de hoofdpijn. Uren voordat de pijn begint - soms al een dag eerder - zijn er subtiele veranderingen die je misschien herkent: je bent onverklaarbaar moe, hebt plotseling trek in zoet, gaapt voortdurend, bent prikkelbaar, of merkt dat concentreren moeilijker gaat dan normaal.
Dit zijn geen willekeurige bijverschijnselen. Ze worden veroorzaakt door vroege activiteit in de hypothalamus , een klein maar buitengewoon invloedrijk hersengebied dat onder andere slaap, eetlust, energiehuishouding en hormonen reguleert.
Op functionele MRI-scans is te zien dat de hypothalamus al actief wordt in deze fase, nog voordat er iets anders waarneembaars gebeurt. De hypothalamus heeft directe verbindingen met het trigeminovasculaire systeem - het systeem dat straks de migraine aanval zal produceren.
Je kunt het beschouwen als een oven die langzaam opwarmt: de temperatuur stijgt al, de warmte is aanwezig, maar het echte bakken begint pas later.
Het aura: een golf van stilte over de hersenschors
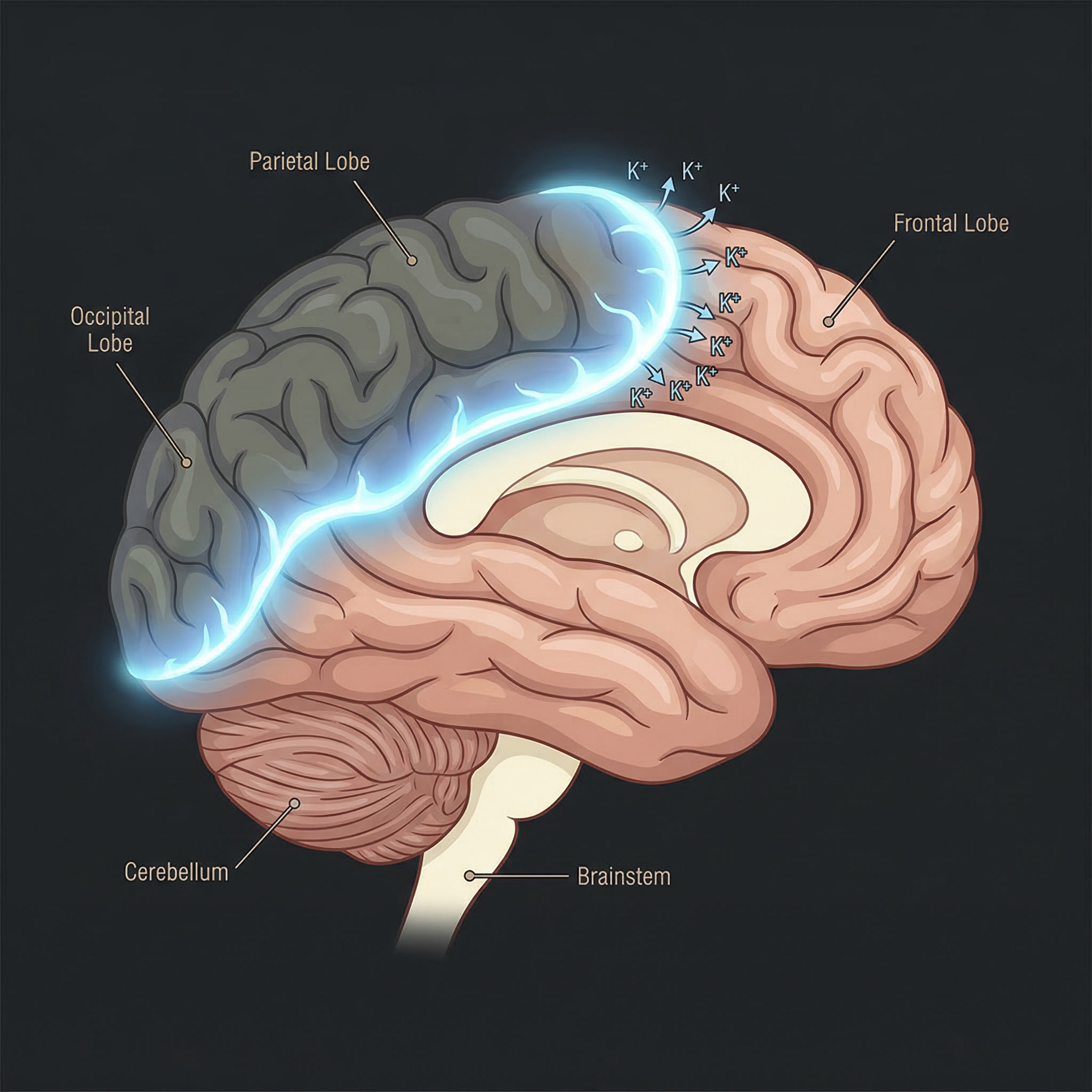
Cortical spreading depression (CSD): een golf van massale elektrische activiteit trekt van achter naar voren over de hersenschors, met een snelheid van twee tot vijf millimeter per minuut. Het donkergrijze gebied links toont de suppressiefase — neuronen die tijdelijk uitgeput zijn na intense activiteit. Aan het wavefront stromen kalium-ionen (K⁺) de extracellulaire ruimte in, het chemische spoor dat de trigeminus-pijnvezels activeert.
Ongeveer een derde van de mensen met migraine ervaart aura, meestal herkenbaar als een flikkerende zigzaglijn of lichtboog in het gezichtsveld, die langzaam uitbreidt en een blinde vlek achterlaat. Dit duurt gewoonlijk twintig tot zestig minuten, verdwijnt dan vanzelf, en de hoofdpijn volgt.
Twee derde van mensen met migraine heeft geen aura, en toch wil ik deze wel bespreken, want wat er in de hersenen tijdens het aura gebeurt is fascinerend en redelijk dramatisch:
Een golf van massale elektrische activiteit spoelt over de hersenschors, van achter naar voren, met een snelheid van twee tot vijf millimeter per minuut. Achter bevindt zich de visuele cortex, vandaar de symptomen in het gezichtsveld bij sommigen.
In het kielzog van die golf raken neuronen tijdelijk uitgeput - ze zijn zo intensief actief geweest dat ze even in een soort 'elektrische schuld' zitten en niets meer kunnen. De activiteit valt stil.
Dit proces heet cortical spreading depression (CSD), ofwel corticaal spreidende depressie, wat klinkt als een Scandinavische gemoedsaandoening, maar simpelweg een technische beschrijving is van een depolarisatiegolf gevolgd door suppressie, de onderdrukking van prikkels.
Terwijl die golf over de visuele cortex trekt, zie je als patient het aura. Heel soms, minder dan een procent, treft de golf ook andere gebieden -de somatosensorische cortex, de taalgebieden, de motorische schors- zodat er tijdelijk tintelingen in de hand optreden, moeite met spreken, of zelfs een voorbijgaand krachtsverlies aan één kant van het lichaam.
Begrijpelijkerwijs alarmerend als je het voor het eerst meemaakt, en onderscheiden van een TIA is klinisch relevant - vandaar dat nieuw optredend aura met motorische uitval altijd door een arts beoordeeld moet worden.
Die elektrische golf laat ook een chemisch spoor na. Kalium-ionen stromen massaal de extracellulaire ruimte in, vergezeld van protonen, glutamaat, ATP en diverse ontstekingsmediatoren. Dit chemische mengsel is precies de brug naar wat de hoofdpijn veroorzaakt, want het bereikt de pijnzenuwen die langs de meningeale bloedvaten lopen.
Waarom doet het pijn? De trigeminus als overbrenger van slecht nieuws
De hersenen zelf hebben geen nociceptoren, ze kunnen geen pijn voelen. Daarom kunnen er ook redelijk straffeloos stimulatoren bij bijvoorbeeld de ziekte van Parkinson achtergelaten worden.
Maar de hersenvliezen, met name de dura mater (het stevige buitenste vlies dat de hersenen omhult), zijn wél uitgebreid geïnnerveerd met nociceptoren. Deze worden verzorgd door de nervus trigeminus, de grote gevoelszenuw van het hoofd en gezicht, waarvan de eerste tak (V1, de oogtak) langs de meningeale bloedvaten loopt.
Wanneer de chemische nasleep van de corticale spreidende depressie (CSD) - kalium-ionen, protonen, glutamaat en diverse ontstekingsmediatoren - de trigeminovasculaire nociceptoren in de dura mater bereikt, worden deze nociceptoren geactiveerd. Ze beginnen te vuren en sturen signalen richting het centrale zenuwstelsel: "er is iets aan de hand, dit moet worden doorgegeven".
Tegelijkertijd vertonen deze zenuwvezels een uniek kenmerk dat migraine onderscheidt van andere pijnervaringen: antidrome oftewel retrograde activiteit.
Dat betekent dat ze signalen niet alleen naar het brein sturen, maar ook terug naar hun perifere uiteinden in de meningeale bloedvatwand. Daar geven ze neuropeptiden vrij, waarvan CGRP het belangrijkste is.
Deze stoffen veroorzaken vasodilatatie en lokale ontstekingsreacties, waardoor de nociceptoren zelf nog prikkelbaarder worden en het pijnsignaal verder wordt versterkt.
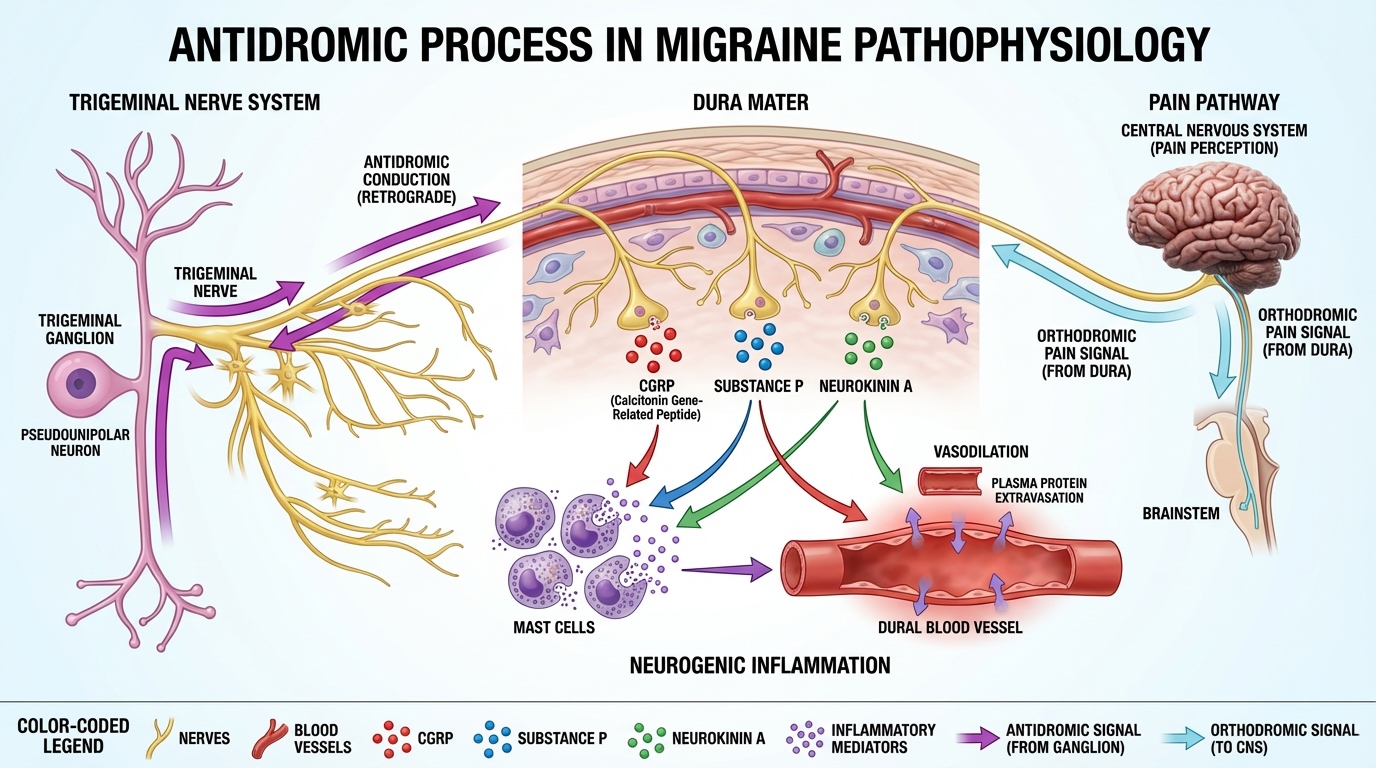
ANTIDROMIC PROCESS IN MIGRAINE PATHOPHYSIOLOGY
Beschrijving infographic:
1. Trigeminussysteem (links) — het trigeminus ganglion met pseudo-unipolaire neuronen
2. Antidrome geleiding (paarse pijlen) — retrograde signaaloverdracht van het trigeminus ganglion naar de perifere zenuwuiteinden in de dura mater
3. Neuropeptide-afgifte — CGRP (rood), substance P (blauw) en neurokinine A (groen) vrijgekomen aan de zenuwuiteinden
4. Neurogene ontsteking — degranulatie van mestcellen met vrijkomen van ontstekingsmediatoren
5. Vasodilatatie — verwijding van durale bloedvaten met extravasatie van plasma-eiwitten
6. Pijnpathway (cyaan pijlen) — orthodrome signaaloverdracht terug via de hersenstam naar het centraal zenuwstelsel voor pijnperceptie
De kleurgecodeerde legenda onderaan helpt de verschillende onderdelen van elkaar te onderscheiden. Deze infographic is gebaseerd op bevindingen uit 79 peer-reviewed publicaties over de pathofysiologie van migraine.
Deel 2: CGRP — het molecuul dat migraine definieert
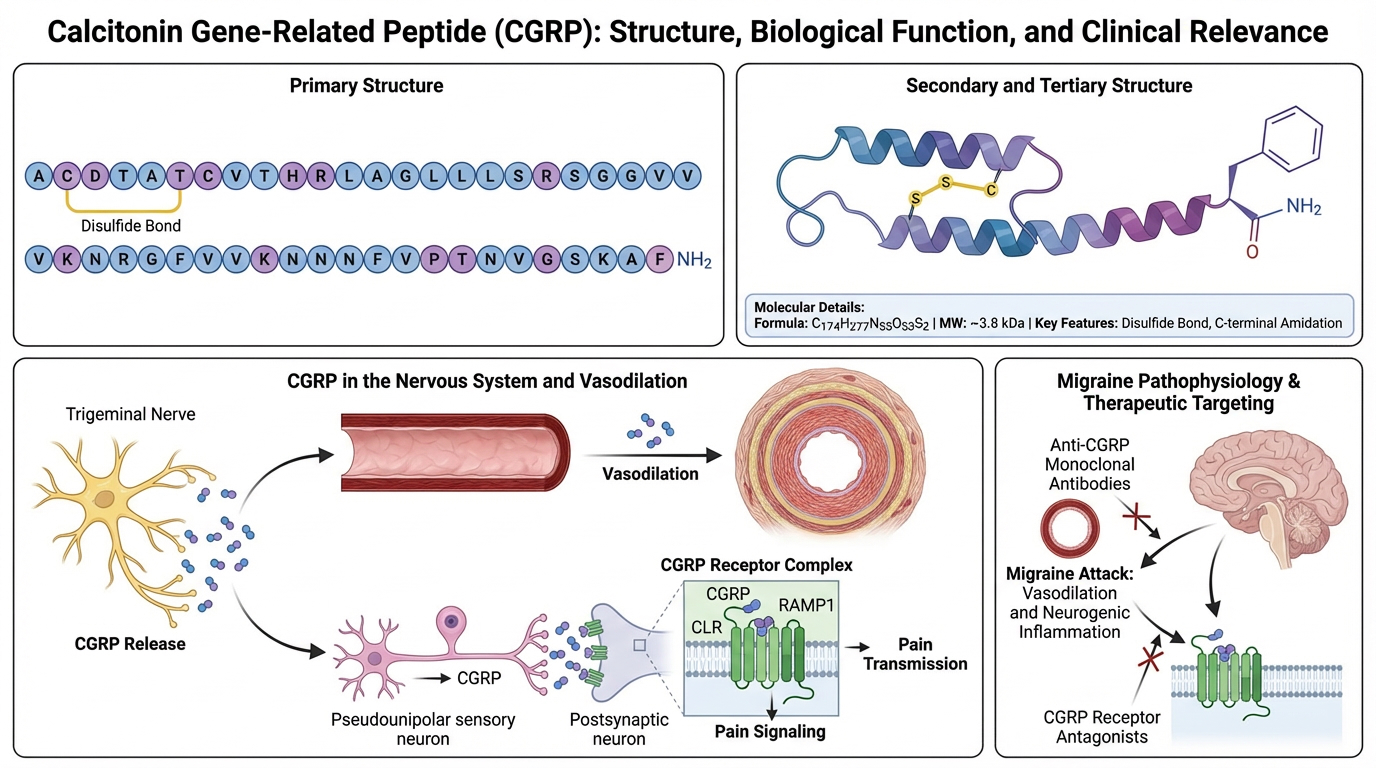
Van boven van links naar rechts:
Primary Structure - The complete 37 amino acid sequence showing the characteristic disulfide bond between cysteine residues at positions 2 and 7
Secondary/Tertiary Structure - The 3D conformation highlighting:
Alpha-helix regions
The critical disulfide bridge
C-terminal amidation
Molecular details (formula: C₁₄₉H₂₄₀N₄₆O₄₇S₂, MW: 3789.3 Da)
Biological Context - CGRP's role in:
Trigeminal nerve signaling
Vasodilation of blood vessels
Receptor complex (CLR/RAMP1) interaction
Pain transmission pathways
Clinical Relevance - Its involvement in migraine pathophysiology and therapeutic targeting strategies
CGRP (calcitonin gene-related peptide) is een klein eiwit van 37 aminozuren dat een centrale rol speelt bij migraine — zo centraal dat de gehele modernste generatie migrainebehandelingen erop gericht is het te blokkeren.
De ontdekking van CGRP's rol in migraine, in de jaren tachtig en negentig, heeft decennia later geleid tot de meest effectieve migrainebehandeling die we ooit hebben gehad. Wetenschap heeft soms een lange aanloop nodig, er is dan soms ook een prachtige landing.
Wat CGRP doet
CGRP wordt opgeslagen in de trigeminus-zenuwvezels die langs de meningeale bloedvaten lopen. Wanneer die vezels geactiveerd worden - door het 'chemisch afval' van een CSD, of door andere triggers - maken ze CGRP vrij.
Dat CGRP heeft meerdere effecten:
Ten eerste: vasodilatatie. CGRP bindt aan receptoren op de wand van de meningeale bloedvaten en zorgt ervoor dat die bloedvaten wijder worden. Die vasodilatatie versterkt op zijn beurt de mechanische prikkeling van de pijnvezels die langs die vaten lopen - een uitgerekt bloedvat trekt aan zijn omgeving - en draagt bij aan de kloppende, pulserende aard van de migrainepijn.
Ten tweede: een feedforward-loop via stikstofmonoxide. CGRP activeert ook de endotheelcellen in de bloedvatwand, die daardoor stikstofmonoxide (NO) aanmaken. NO diffundeert terug naar de trigeminus-zenuwvezeluiteinden en stimuleert die - je raadt het al - om nog meer CGRP los te laten. Het is een zichzelf versterkend systeem, wat verklaart waarom een migraineaanval, eenmaal op gang, niet vanzelf stopt als je er gewoon doorheen probeert te werken.
Ten derde: sensitisatie van naburige zenuwvezels. CGRP bindt ook aan receptoren op de dikkere, gemyeliniseerde Aδ-vezels naast de dunne C-vezels die het initieel vrijlaten. Daardoor worden ook die vezels gevoeliger: de pijndrempel daalt, en het gebied waarover pijn wordt gevoeld breidt zich uit.
De sensitisatie beperkt zich niet tot alleen de perifere vezels maar reikt tot in het ganglion zelf: De trigeminus-zenuwcellen hebben hun cellichamen niet in het brein, maar in het trigeminus ganglion, een soort verzamelknoop halverwege de weg tussen de perifere uiteinden in de meninges en de centrale projecties naar de trigeminuskernen in de hersenstam.
CGRP wordt ook dáár vrijgelaten , in het ganglion, en werkt paracrien , dat wil zeggen het beïnvloedt naburige zenuwcellen en de zogenaamde satelliet-gliacellen rondom hen.
Het gevolg: de perifere sensitisatie breidt zich uit, ook zonder dat er nog een actieve aanval gaande is. Dit is een van de mechanismen die verklaren waarom migraine zich chronisch kan ontwikkelen.
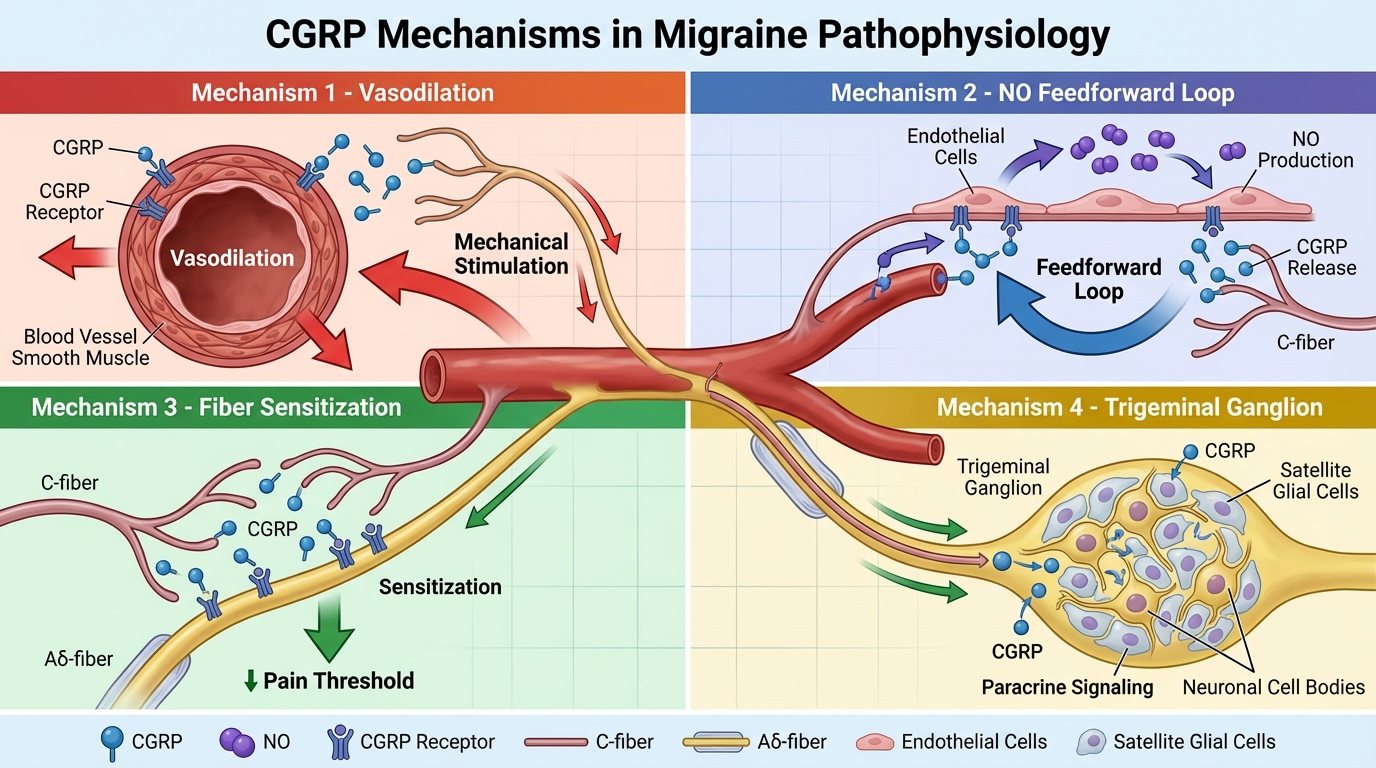
De CGRP-receptor
CGRP bindt aan een receptor die bestaat uit twee eiwitten die samenwerken: CLR (calcitonin receptor-like receptor) en RAMP1 (receptor activity-modifying protein 1).
RAMP1 is als een sleutel die de functie van CLR bepaalt: zonder RAMP1 zou CLR een heel ander molecuul binden. Dit receptor-complex is het farmacologische doelwit voor de nieuwste migrainebehandelingen.
Een verwant receptor-complex, AMY1 (ook CLR maar dan met RAMP1 in een andere configuratie), heeft overlappende farmacologie — wat betekent dat sommige behandelingen mogelijk iets breder werken dan alleen via de klassieke CGRP-receptor. Of dat klinisch relevant is, is nog onderwerp van onderzoek.
CGRP als bewijs voor de oorzaak
Een van de mooiste bewijsstukken voor de rol van CGRP in migraine is provocatief van aard: als je bij mensen met migraine CGRP intraveneus toedient, krijgt een fors deel van hen een migraineaanval. Dit is een van de sterkste argumenten dat CGRP niet een gevolg is van migraine, maar een oorzaak.
En het feit dat antilichamen die CGRP blokkeren, en die de bloedhersenbarrière nauwelijks passeren, dus voornamelijk perifeer werken, dat die antilichamen zo effectief zijn bij het voorkomen van aanvallen, bevestigt het volgende: de kritische pathologie speelt zich af in de periferie, niet diep in de hersenen.
Deel 3: Van periferie naar centraal — hoe de pijn versterkt wordt
Het trigeminovasculaire systeem: anatomie van de aanval
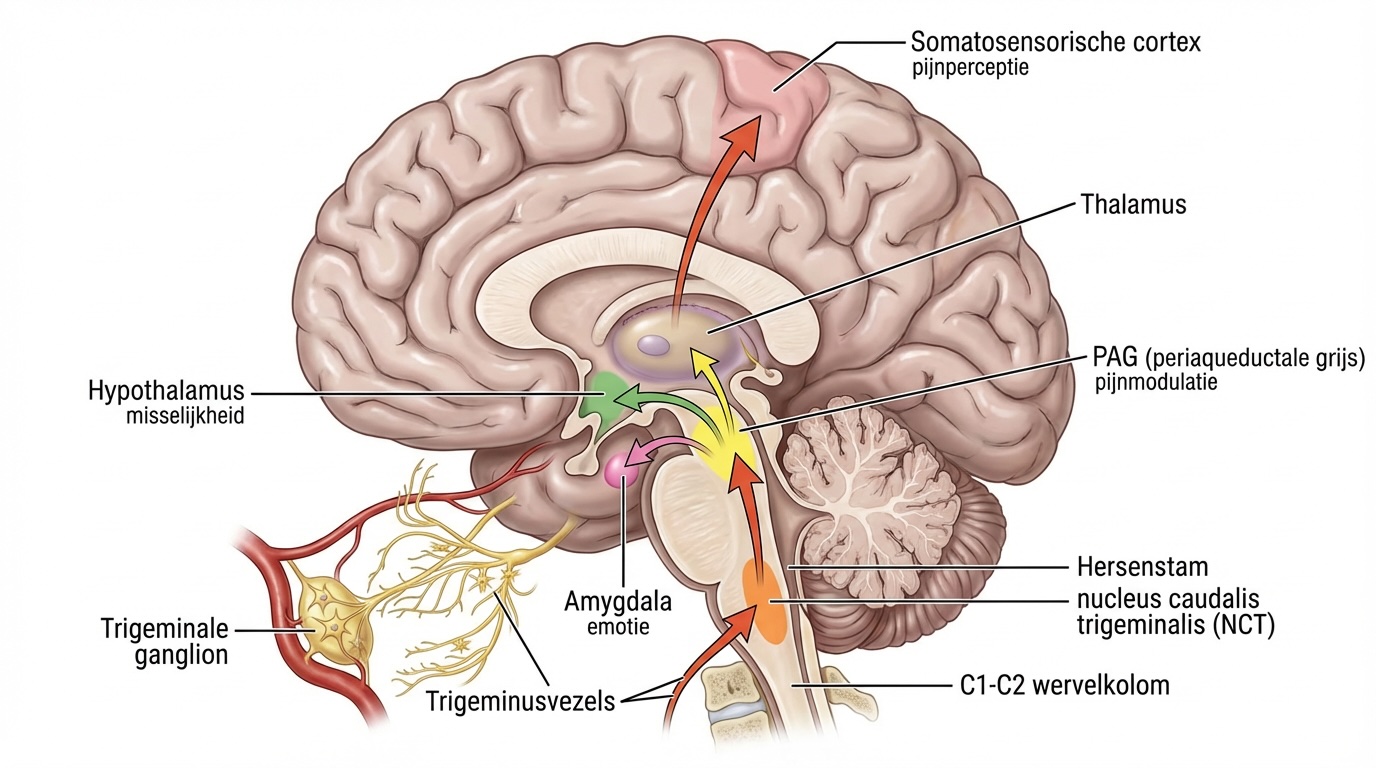
De geactiveerde trigeminusvezels sturen hun pijnsignalen niet rechtstreeks naar de bewuste pijnperceptie. Ze reizen eerst naar de nucleus caudalis trigeminalis (NCT) — een kern in de onderkant van de hersenstam en het bovenste ruggenmerg (ter hoogte van C1-C2).
Functioneel is de NCT vergelijkbaar met de dorsale hoorn van het ruggenmerg voor de rest van het lichaam: het is de eerste schakelpost waar signalen vanuit nociceptoren aankomen vanuit de periferie en worden doorgegeven aan hogere hersengebieden.
Vanuit de NCT gaan de signalen verder naar de thalamus (het centrale knooppunt voor sensorische informatie uit het lichaam en het hoofd) en vandaar naar de somatosensorische cortex — waar de bewuste pijnperceptie plaatsvindt.
Maar er zijn ook verbindingen naar de hypothalamus, de periaqueductale grijs (PAG, een gebied dat pijn kan moduleren), en de amygdala. Dat verklaart waarom migraine niet alleen pijn is, maar ook angst, emotionele reactiviteit, misselijkheid, en een verstoord gevoel van algeheel welbevinden met zich meebrengt.
Perifere sensitisatie: het alarm staat open
Na de eerste activatie van de trigeminus-pijnvezels treedt perifere sensitisatie op: de drempel waarop die vezels vuren is nu verlaagd.
Ze reageren op prikkels die normaal gesproken geen pijn zouden veroorzaken, en ze reageren heviger op prikkels die normaal licht ongemak zouden geven. Klinisch herkenbaar als allodynie van hoofd en gezicht — het voelt pijnlijk aan om je haar aan te raken, een hoed te dragen, of je gezicht te wassen.
Niet omdat er schade is, maar omdat het alarmsysteem nu ook reageert op onschuldige aanrakingen.
Centrale sensitisatie: de versterker staat te hoog
Als de aanval lang genoeg duurt, of als aanvallen frequent terugkeren, kan sensitisatie zich uitbreiden naar de tweede en derde orde neuronen in de NCT en de thalamus. Dit is centrale sensitisatie: de neuronen in het centraal zenuwstelsel zelf reageren nu overdreven.
Een klinisch teken hiervan is cutane allodynie die zich uitbreidt voorbij het hoofd , ook aanrakingen op de arm of het been worden als pijnlijk of onaangenaam ervaren tijdens de aanval. Dit is een teken dat de sensitisatie de thalamus heeft bereikt.
Dit heeft een directe therapeutische implicatie: triptanen en andere acute middelen werken het best als ze worden ingenomen voordat centrale sensitisatie is opgetreden. Is de centrale sensitisatie eenmaal aanwezig - wat in de praktijk betekent: na een uur of twee van actieve aanval (!) - dan verliest acute behandeling fors aan effectiviteit.
Vroeg behandelen van een migraine aanval is geen ongeduld, het is neurobiologie. De verstandigste strategie dus, en niet 'kijken of het misschien toch overgaat' voordat je medicatie neemt.
Van episodisch naar chronisch: wanneer het systeem niet meer terugkeert naar nul
Bij de meeste mensen herstelt het zenuwstelsel zich tussen aanvallen in volledig. Maar bij een deel van de migrainepatiënten treedt geleidelijk ‘chronificatie' op: de aanvallen worden frequenter, de drempel lager, en op een gegeven moment zijn er meer dan vijftien hoofdpijndagen per maand, waarvan minimaal acht voldoen aan de criteria voor migraine. Dit heet chronische migraine.
Waarschijnlijk zijn er meerdere mechanismen die dit proces aandrijven.
Ten eerste is er de eerdergenoemde perifere sensitisatie in het trigeminus ganglion, waarbij satelliet-gliacellen langdurig geactiveerd blijven (ook tussen de aanvallen door) waardoor het systeem niet volledig tot rust komt.
Ten tweede is er de shift in centrale sensitisatie: van activiteitsafhankelijk (de sensitisatie treedt op tijdens een aanval en verdwijnt daarna) naar activiteitsonafhankelijk (de sensitisatie is permanent aanwezig, ongeacht of er een aanval gaande is).
Dit markeert de overgang van episodische naar chronische migraine.
Een derde factor is overgebruik van medicatie: het frequent gebruik van pijnstillers en triptanen (meer dan tien behandeldagen per maand) leidt paradoxaal genoeg tot een verlaging van de aanvalsdrempel, en dus een verhoogde gevoeligheid.
Het brein past zich aan het voortdurend blokkeren van pijnsignalen aan door meer pijnreceptoren aan te maken en de nociceptieve paden gevoeliger te maken. Het resultaat is dat de medicatie die je gebruikt om de pijn te bestrijden, bijdraagt aan het chronificeren van de aandoening.

Dit is geen onwil of zwakte van de patiënt, het is neuroplastische aanpassing : het zenuwstelsel compenseert voor de voortdurende blokkade door meer receptoren te produceren en de signaalversterking op te schroeven.
Zo werkt medicatieovergebruik bij migraine: wat eerst verlichting bracht, maakt het pijnsysteem op den duur juist hypergevoelig, waardoor aanvallen vaker en chronischer worden.
Deel 4: Behandeling — van acute aanval tot preventie
Acute behandeling: de aanval stoppen
Gewone pijnstillers en ontstekingsremmers
Bij een milde tot matig heftige aanval grijpen veel mensen naar paracetamol of een ontstekingsremmer zoals ibuprofen of naproxen - de zogenaamde NSAID's. Die laatste categorie verdient wat meer uitleg, want ze doen iets specifieks dat bij migraine relevant is.
NSAID's blokkeren het enzym cyclo-oxygenase (COX), dat prostaglandines produceert. Prostaglandines zijn signaalstoffen die pijn versterken en ontstekingsreacties bevorderen, en bij migraine maken ze de pijnvezels in de hersenvliezen extra gevoelig voor prikkels. Blokkeer je de aanmaak, dan daalt die verhoogde gevoeligheid. Vroeg innemen is daarbij geen detail: hoe eerder in de aanval, hoe effectiever.
Cafeïne maakt het combinatieplaatje interessanter. Sommige mensen merken dat een sterke kop koffie aan het begin van een aanval verlichting geeft - dat is geen toeval. Cafeïne blokkeert adenosinereceptoren in het brein, wat vaatverwijding tegengaat en de pijnstillende werking versterkt.
Twee decennia onderzoek laten consistent zien dat de combinatie paracetamol-aspirine-cafeïne effectiever is dan de losse middelen afzonderlijk, en vaak ook sneller werkt dan ibuprofen alleen. Of het even goed werkt als triptanen is lastig te zeggen - de vergelijkende studies zijn schaars en te verschillend van opzet voor harde conclusies - maar de combinatie draagt substantieel bij.
Cafeïne heeft wel een keerzijde: nervositeit en hartkloppingen komen vaker voor, en bij regelmatig gebruik stijgt het risico op medicatie-overgebruikshoofdpijn. Dat risico geldt overigens voor alle acute migrainemiddelen bij te frequent gebruik, cafeïne is daarin niet uniek, alleen wat minder bekend.
Dan de misselijkheidsremmers, want die doen meer dan je zou verwachten. Metoclopramide en domperidon worden niet alleen gegeven tegen de misselijkheid zelf. Tijdens een migraineaanval vertraagt de maag door verstoorde vagale regulatie: medicatie die je slikt wordt daardoor slecht opgenomen, soms nauwelijks. Door de maagmotiliteit te herstellen zorgen deze middelen ervoor dat andere medicatie überhaupt de kans krijgt om te werken. Metoclopramide lijkt bovendien een klein direct effect op de hoofdpijn te hebben, waarschijnlijk via interactie met serotonine- en dopaminesystemen, al is het mechanisme niet volledig opgehelderd.
Triptanen: de eerste specifieke migrainebehandeling
De ontwikkeling van triptanen in de jaren tachtig en negentig betekende een doorbraak. Paracetamol en ibuprofen pakken pijn aan. Triptanen pakken migraine aan. Dat klinkt als een subtiel onderscheid, maar het is fundamenteel. Want voor het eerst was er medicatie die niet symptomen dempte, maar ingreep op het proces zelf.
Triptanen binden aan twee typen serotonine-receptoren: 5-HT1B en 5-HT1D. Die zitten op strategische plekken in het trigeminovasculaire systeem, en dat is precies waarom ze zo effectief zijn. Via de 5-HT1B-receptor vernauwen ze de meningeale bloedvaten en draaien ze de CGRP-gedreven vasodilatatie terug. Via de 5-HT1D-receptor remmen ze de trigeminale zenuwuiteinden direct, waardoor minder CGRP vrijkomt en het pijnsignaal richting hersenstam afneemt. Vasculair én neuraal tegelijk - een dubbele aanpak op twee niveaus van dezelfde cascade.
Er bestaan zeven varianten die farmacologisch sterk op elkaar lijken maar verschillen in snelheid en werkingsduur. Eletriptan en rizatriptan beginnen sneller te werken. Sumatriptan en zolmitriptan zijn wat trager maar hebben het meeste onderzoeksbewijs achter zich. Sumatriptan gecombineerd met naproxen presteert beter dan elk van beide afzonderlijk: de triptaan remt de trigeminale pijnbaan, het NSAID pakt de prostaglandine-gemedieerde sensitisatie aan. Twee mechanismen, één aanval.
Timing is geen bijzaak. Triptanen werken het best vóórdat centrale sensitisatie optreedt — dus vroeg in de aanval. Na anderhalf tot twee uur actieve aanval daalt de kans op volledige pijnverlichting merkbaar. Dat is dezelfde reden waarom vroeg behandelen verstandig is: niet ongeduld, maar neurobiologie.
De keerzijde is onlosmakelijk verbonden met het werkingsmechanisme. De vaatvernauwing die triptanen zo effectief maakt, is precies wat ze ongeschikt maakt voor mensen met hart- of vaatziekten, ongecontroleerde hypertensie of een doorgemaakte beroerte. Hetzelfde mechanisme dat de aanval doorbreekt, kan bij kwetsbare bloedvaten problemen veroorzaken. En net als andere acute middelen geldt: meer dan tien behandeldagen per maand, en het middel dat aanvallen stopt wordt zelf een trigger voor nieuwe aanvallen.
Ditans: "triptanen zonder vaatvernauwing"
Lasmiditan lost één specifiek probleem op: wat geef je mensen voor wie triptanen te riskant zijn vanwege hart- of vaatziekten?
Het antwoord zat in een ander receptortype. Lasmiditan werkt via de 5-HT1F-receptor, die voorkomt in de hersenvliezen, hypothalamus, thalamus, cortex en aan de uiteinden van trigeminuszenuwen. Via die receptor remt het de vrijzetting van CGRP en blokkeert het glutamaatoverdracht in de trigeminus-terminals. Cruciaal verschil met triptanen: het vernauwt de bloedvaten niet. Het cardiovasculaire bezwaar vervalt.
Lasmiditan lost goed op in vet en passeert daardoor gemakkelijk de bloed-hersenbarrière — wat verklaart waarom het zo effectief centraal werkt. In werkzaamheid is het vergelijkbaar met triptanen. Maar dat centrale effect heeft een prijs: het middel maakt slaperig, en een kwart van de gebruikers wordt duizelig. Na inname is autorijden minimaal acht uur niet veilig.
Voor iemand die midden op een werkdag een aanval wil doorbreken is dat een reëel probleem. Lasmiditan staat dan ook als derde keus in de meeste richtlijnen. Niet omdat het slecht werkt, maar omdat de bijwerkingen de toepasbaarheid beperken. Het vult een belangrijke niche voor wie cardiovasculaire contra-indicaties heeft, maar het vervangt triptanen niet universeel.
Gepants: de CGRP-receptorblokkers
Waar triptanen en ditans inwerken op serotonine-receptoren, gaan gepants een stap verder terug in de cascade. Ze blokkeren de CGRP-receptor rechtstreeks: de CLR/RAMP1-combinatie waarover deel 2 ging. Ze nemen de plek in waar CGRP normaal zou binden, maar activeren de receptor zelf niet. Geen CGRP-signaal, geen vasodilatatie, geen sensitisatie via die route.
Voor acute behandeling zijn ubrogepant, rimegepant en zavegepant beschikbaar, waarbij die laatste als neusspray komt.
Net als lasmiditan vernauwen ze bloedvaten niet en zijn ze daarmee cardiovasculair veilig.
Maar ze hebben nog een voordeel dat de andere klassen missen: ze veroorzaken geen medicatie-overgebruik. Je kunt ze vaker inzetten zonder dat ze zelf aanvallen gaan uitlokken, al blijft profylaxe zinvoller dan de acute dosis steeds ophogen bij frequente aanvallen.
Rimegepant heeft een bijzonder profiel. Het is het enige middel dat zowel acute aanvallen kan stoppen als profylactisch werkt. Bovendien lijkt het al effectief te zijn wanneer je het in de prodromale fase neemt, nog voordat de hoofdpijn begint. Voor wie zijn prodroom goed leert herkennen is dat een relevant voordeel.
De veiligheidssignalen verdienen aandacht. Wederom geen werking zonder bijwerking: Rimegepant is in de klinische praktijk geassocieerd met huidreacties en soms haaruitval. Atogepant, een verwant gepant dat ook preventief werkt, geeft relatief vaak obstipatie. In de WHO farmacovigilantie-database is het Raynaud-fenomeen gemeld als mogelijk klasse-effect, al is het signaal klein. Redenen om bijwerkingen te melden en alert te blijven, geen redenen om de middelen te mijden.
Nederland heeft lang gewacht met vergoeding van CGRP-remmers. Sinds november 2025 worden ze vergoed bij chronische migraine zonder medicatie-overgebruik, nadat eerst topiramat, valproaat en twee behandelingen met botox zijn geprobeerd. Voor episodische migraine geldt vergoeding na vijf eerdere profylactische middelen.
Overzicht migraine medicatie
| Klasse | Voorbeelden | Aangrijpingspunt | CV veilig | Overgebruiksrisico | Acuut | Profylaxe |
|---|---|---|---|---|---|---|
| NSAID's | Ibuprofen, naproxen, aspirine | COX-remming → minder prostaglandines | Beperkt | Ja | Ja | Nee |
| Triptanen | Sumatriptan, eletriptan, rizatriptan | 5-HT1B/1D agonist → vasoconstrictie + CGRP-remming | Nee | Ja | Ja | Nee |
| Ditans | Lasmiditan | 5-HT1F agonist → CGRP-remming, geen vasoconstrictie | Ja | Onduidelijk | Ja | Nee |
| Gepants (acuut) | Ubrogepant, rimegepant, zavegepant | CGRP-receptorblokker | Ja | Nee | Ja | Rimegepant |
| Gepants (profylaxe) | Atogepant, rimegepant | CGRP-receptorblokker | Ja | Nee | Rimegepant | Ja |
| Anti-CGRP antilichamen | Erenumab, fremanezumab, galcanezumab, eptinezumab | CGRP-molecuul of -receptor blokkeren | Voorzichtig bij CV-risico | Nee | Nee | Ja |
| Botulinetoxine | OnabotulinumtoxineA | SNARE-blokkade → minder CGRP-afgifte perifeer | Ja | Nee | Nee | Alleen chronisch |
CV veilig = cardiovasculair veilig bij hart- en vaatziekten. Overgebruiksrisico = kans op medicatie-overgebruikshoofdpijn bij frequent gebruik.
Profylactische behandeling: de aanvallen voorkomen
Acute medicatie stopt een aanval. Profylaxe verandert het systeem erachter.
Profylaxe wordt overwogen wanneer migraine je leven substantieel verstoort. De internationale richtlijnen hanteren als vuistregel vier of meer migrainedagen per maand met significante beperkingen, of acht of meer dagen ongeacht de ernst. Ook bij onvoldoende effect van acute behandeling of dreigend medicatie-overgebruik komt profylaxe in beeld.
Het gestelde doel klinkt bescheiden: de aanvallen halveren, niet elimineren. Maar dat is realistischer dan het lijkt. Van twaalf naar zes migrainedagen per maand is het verschil tussen chronische invaliditeit en een hanteerbaar bestaan. Volledige controle gebeurt soms, maar is geen redelijk startpunt voor de verwachting.
Bij episodische migraine geldt halvering van het aantal aanvalsdagen als succes. Bij chronische migraine is dertig procent reductie al het criterium. Dat verschil weerspiegelt hoe moeilijk chronische migraine te behandelen is, niet hoe laag de lat ligt.
De klassieke profylaxe: middelen uit andere vakgebieden
De traditionele profylactische middelen werden oorspronkelijk voor andere aandoeningen ontwikkeld. Bètablokkers voor hartklachten, anticonvulsiva voor epilepsie, antidepressiva voor stemming. Dat ze ook migraine behandelen is deels toeval, deels een reflectie van hoe sterk neurotransmittersystemen overlappen tussen verschillende aandoeningen. GABA, serotonine, noradrenaline spelen overal een rol.
Propranolol heeft het meeste bewijs van alle bètablokkers. Het werkt goed, maar hoe precies is verrassend onduidelijk voor iets dat al decennia wordt voorgeschreven. Waarschijnlijk moduleert het de trigeminovasculaire pathway via noradrenaline, mogelijk via de locus coeruleus, een hersengebied dat noradrenaline afgeeft en pijnmodulatie beïnvloedt. Bijwerkingen zijn bekend: moeheid, koude extremiteiten, soms nachtmerries. Bij astma of ernstige doorbloedingsstoornissen is het niet geschikt.
Topiramaat werkt via meerdere routes tegelijk: blokkade van natriumkanalen, versterking van remmende GABA-signalering, remming van stimulerende glutamaatreceptoren, en blokkade van koolzuuranhydrase. In diermodellen verhoogt het de drempel voor corticale spreidende depressie.
Het effect is aangetoond, maar de bijwerkingen zijn berucht: cognitieve vertraging, tintelingen, gewichtsverlies. Cruciaal: topiramaat is sterk teratogeen en mag niet worden gebruikt bij wie zwanger kan worden zonder waterdichte anticonceptie en uitgebreide counseling vooraf.
Valproaat deelt mechanismen met topiramat: blokkade van ionenkanalen, GABA-versterking, mogelijk remming van corticale spreidende depressie. Het werkt, maar is nog sterker teratogeen dan topiramat. Leverbelasting en gewichtstoename komen erbij. Het wordt daardoor steeds minder als eerste keus gebruikt, zeker bij vrouwen die zwanger kunnen worden.
Amitriptyline remt de heropname van serotonine en noradrenaline, blokkeert natriumkanalen en werkt antihistaminerg. Het helpt bij migraine, vooral bij chronische vormen en bij wie ook spanningshoofdpijn of slaapproblemen heeft. De doseringen die nodig zijn liggen veel lager dan voor de behandeling van depressie. Droge mond, slaperigheid en gewichtstoename komen vaak voor.
Flunarizine blokkeert calciumkanalen en remt dopamine-D2-receptoren enigszins. In Nederland is het specifiek geregistreerd voor migraine. Het werkt, maar gewichtstoename en somberheid zijn frequent. Bij langdurig gebruik bestaat risico op bewegingsstoornissen die lijken op parkinsonisme. Voor wie al depressieve klachten heeft is het niet de beste keus.
Candesartan en lisinopril, respectievelijk een angiotensineblokker en een ACE-remmer, werken verrassend goed preventief. Hoe precies is niet volledig opgehelderd; mogelijk speelt het angiotensinesysteem een rol in centrale pijnmodulatie. Ze zijn een logische keus bij wie ook hypertensie heeft.
Magnesium remt NMDA-receptoren en beïnvloedt ionenkanalen. Het effect is bescheiden, maar de veiligheid uitstekend. Het is een van de weinige middelen die ook tijdens zwangerschap verdedigbaar zijn.
Anti-CGRP monoklonale antilichamen: de revolutie
Alle klassieke profylactische middelen hebben één ding gemeen: ze werden niet voor migraine ontwikkeld. De monoklonale antilichamen wel. Dat is geen marketingclaim, en het verklaart wel waarom ze anders presteren dan alles wat eraan voorafging.
Tussen 2018 en 2021 kwamen vier middelen beschikbaar: erenumab, fremanezumab, galcanezumab en eptinezumab.
Erenumab blokkeert de CGRP-receptor zelf. De andere drie blokkeren het CGRP-molecuul voordat het de receptor bereikt. Klinisch maakt dat verschil nauwelijks, al heeft erenumab theoretisch een iets breder effect omdat het ook de AMY1-receptor blokkeert, een verwante receptor die mogelijk bij migraine betrokken is.
Ze worden toegediend als subcutane injectie of intraveneus infuus, maandelijks of per kwartaal afhankelijk van het middel. Ongeveer de helft van de gebruikers krijgt halvering van het aantal migrainedagen. Een kwart haalt vijfenzeventig procent reductie of meer. Die cijfers lijken bescheiden totdat je beseft dat deze middelen ook werken bij wie al meerdere klassieke profylactische middelen heeft geprobeerd zonder succes.
Dat is het punt waar ze echt van traditionele profylaxe afwijken. Klassieke middelen hebben zoveel overlap in werkingsmechanisme dat een derde poging na twee mislukkingen weinig kans van slagen heeft. Monoklonale antilichamen doorbreken dat patroon omdat ze een fundamenteel ander aangrijpingspunt hebben.
Er is één waarschuwing die aandacht verdient, met name voor wie vasculair risico heeft. CGRP doet in het lichaam meer dan migraine veroorzaken: het verwijdt bloedvaten en speelt een beschermende rol bij hersenischemie door collaterale doorbloeding te verbeteren en neuronen in ischemische gebieden te beschermen tegen celdood. Bij wie recent een beroerte of TIA heeft gehad is CGRP-blokkade theoretisch zorgelijk: je remt een beschermend mechanisme. Gegevens uit de klinische praktijk laten zien dat wie goed reageert op monoklonale antilichamen een lagere cerebrale bloedstroomsnelheid heeft, een indirecte aanwijzing voor verminderd collateraalvermogen.
Dit is geen absolute reden om de middelen te mijden, maar wel voor goed overleg met een neuroloog.
In farmacovigilantiedata is erenumab geassocieerd met hypertensie, galcanezumab met atriumfibrilleren en myocardinfarct. Die signalen kwamen niet uit de grote trials, maar die trials sloten mensen met cardiovasculaire problemen bewust uit. Hoe veilig deze middelen op lange termijn zijn bij risicopatiënten is nog niet volledig duidelijk.
Gepants als profylaxe
Atogepant en rimegepant zijn ook goedgekeurd voor preventief gebruik, dagelijks of om de dag oraal ingenomen. Dat is relevant voor wie liever tabletten slikt dan zich injecteert, of bij wie monoklonale antilichamen niet beschikbaar of vergoedbaar zijn.
Rimegepant heeft daarbij een praktisch voordeel: het is hetzelfde middel dat ook acute aanvallen stopt. Eén middel voor twee doelen kan de behandeling vereenvoudigen, zeker voor wie moeite heeft met complexe medicatieschema's.
De ervaring met gepants als profylaxe is nog beperkter dan met monoklonale antilichamen, simpelweg omdat ze recenter zijn. Trials laten vergelijkbare werkzaamheid zien als klassieke profylaxe. Of ze ook werken bij wie meerdere andere middelen heeft geprobeerd zonder succes, zoals monoklonale antilichamen dat wel doen, is nog niet duidelijk.
OnabotulinumtoxineA: Botox als migrainebehandeling
Botox tegen migraine klinkt als een gelukkig toeval, en dat is het ook geweest. Maar het werkingsmechanisme is eleganter dan de naam doet vermoeden.
OnabotulinumtoxineA blokkeert het SNARE-complex, een moleculaire structuur die blaasjes met neurotransmitters en neuropeptiden aan het celmembraan laat fuseren om hun inhoud vrij te geven. Door dat complex te remmen in de perifere uiteinden van de trigeminus vermindert de afgifte van CGRP en andere neuropeptiden. Minder CGRP betekent minder neuroinflammatie en minder sensitisatie. Geen vaatvernauwing, geen centrale effecten, puur perifeer.
Belangrijk voorbehoud: botox werkt alleen bij chronische migraine. Bij episodische migraine is het effect niet aangetoond.
Het wordt toegediend volgens het PREEMPT-protocol: 31 injecties verspreid over hoofd, nek en schouders, elke twaalf weken. Het effect wordt pas na drie behandelcycli beoordeeld, wat betekent dat je negen maanden geduld nodig hebt voor een eerlijke evaluatie. Bij de juiste patiënt kan het resultaat aanzienlijk zijn, maar het vraagt commitment aan een langdurig traject.
Deel 5: Behandeling kiezen - waarom maatwerk noodzakelijk is
Migraine is geen standaardaandoening met een standaardbehandeling. Wat bij de ene patiënt uitstekend werkt, faalt bij de ander. Wat voor jou tien jaar geleden hielp, werkt nu misschien niet meer. En wat farmacologisch logisch klinkt, botst in de praktijk soms met bijwerkingen, interacties met andere medicatie, of simpelweg met wat een specifiek lichaam verdraagt.
Dat is geen tekortkoming van de beschikbare behandelingen. Het is een reflectie van hoe complex migraine als aandoening is. De aanvalsfrequentie, de ernst, de aanwezigheid van comorbiditeiten, de medicatiegeschiedenis, een eventuele zwangerschapswens, al deze factoren bepalen mee welk middel zinvol is en welk niet.
Sommige middelen zijn bij bepaalde hartaandoeningen gecontra-indiceerd. Andere zijn sterk teratogeen. Bepaalde combinaties versterken elkaar, andere werken elkaar tegen.
De internationale richtlijnen hanteren vijftig procent reductie in aanvalsfrequentie als succescriterium, niet omdat volledige controle onmogelijk is, maar omdat het een realistisch startpunt is. Sommige mensen bereiken meer. Soms moet er gewisseld worden voordat iets gevonden wordt dat werkt én verdragen wordt.
Wat dit artikel kan doen is het mechanisme uitleggen en de rationale achter behandelkeuzes inzichtelijk maken. Wat het niet kan doen is de afweging maken die een neuroloog met kennis van jouw volledige medische geschiedenis wel kan maken. Begrip van het mechanisme is geen substituut voor die afweging. Het is de voorbereiding erop.
Migrainezorg is maatwerk.
Deel 6: Wat we nog niet weten
Wetenschap is geen afgesloten boek; het is een lopend proces waarbij elke beantwoorde vraag drie nieuwe vragen stelt. Een selectie van wat op dit moment nog open ligt:
- De PACAP-pathway is een opkomend target. PACAP (pituitary adenylate cyclase-activating polypeptide) werkt via een mechanisme dat sterk lijkt op CGRP: het activeert adenylaat cyclase, verhoogt cAMP in bloedvatwandcellen, veroorzaakt vasodilatatie, maar dan via andere receptoren (PAC1, VPAC1/2). Middelen die de PAC1-receptor blokkeren zijn in klinische trials. Mogelijk relevant voor patiënten die niet voldoende reageren op anti-CGRP therapie.
- Prodroombehandeling het innemen van rimegepant al in de prodromale fase, vóór de hoofdpijn- is klinisch interessant maar nog slecht onderbouwd met gecontroleerde studies. De hypothese is logisch: blokkeer de CGRP-cascade voordat die op gang is, en de aanval start niet. Of dit in de praktijk consistent werkt, en hoe je het prodroom betrouwbaar herkent, zijn vragen die nog open staan.
- Combinatieprofylaxe twee profylactica combineren wordt in de kliniek toegepast maar is vrijwel niet onderzocht in gerandomiseerde trials. Één studie naar de combinatie topiramaat en propranolol liet geen voordeel zien ten opzichte van topiramaat alleen. Klinische praktijk loopt hier voor (of achter) op evidence.
- Cardiovasculaire langetermijnveiligheid van monoklonale antilichamen bij risicopatiënten is onvoldoende onderzocht. De gerandomiseerde trials sloten deze groep grotendeels uit. Real-world registers vullen langzaam de kennislacune, maar het zal jaren duren voordat de data robuust genoeg zijn voor definitieve uitspraken.
- Chronificatiemechanismen: op welk punt verandert activiteit-afhankelijke centrale sensitisatie in activiteit-onafhankelijke? Wanneer worden de klachten chronisch? Is er een therapeutisch venster waarin je chronificatie kunt voorkomen door vroeg en agressief profylaxe te starten? Dit zijn vragen met grote klinische relevantie die nog wachten op antwoord.
Slot:
Migraine is een aandoening waarvoor we in de afgelopen tien jaar meer goede behandelingen hebben gekregen dan in de vijftig jaar daarvoor.
De verklarende biologie die tot die behandelingen leidde, geeft ook een duidelijker zelfbeeld aan mensen die er last van hebben: dit is geen kwestie van doorzetten of een goed humeur.
Het is een zenuwstelsel dat anders is afgesteld, een CGRP-systeem dat te makkelijk in gang wordt gezet, en een nociceptieve signaal route die te lang actief blijft.
Dat begrijpen verandert niets aan de pijn van de volgende aanval. Maar het helpt wel om hem in de goede context te plaatsen. En om de behandelkeuzes die daarna komen beter te maken.
Ik wens de lezers veel pijnvrije dagen.

