Wat er de afgelopen 20 jaar anders werd: een zachte introductie
De afgelopen decennia is er veel veranderd in de pijnwetenschap. Dingen die we als jonge dokter deden, schieten nu de tranen van in mn ogen bij de gedachte alleen al.
Vagotomie bij maagzweer anyone? En zo zijn er meer ontwikkelingen. Zoals in de pijngeneeskunde. Een kort overzicht:
Chronische pijn begrijpen: nieuwe wetenschappelijke inzichten uit de afgelopen 20 jaar

De nieuwe kijk
Hoe ons begrip van chronische pijn fundamenteel is veranderd
Vroegah
Oude kijk

Pijn = Schade
Pijn betekent altijd weefselschade of letsel
Herstel = pijnvrij
Als het kapotte weefsel herstelt, verdwijnt de pijn altijd.
Chronische pijn is acute pijn die langer duurt
Als de langer pijn aanhoudt, is die pijn hetzelfde als de pijn die iemand eerst had, alleen gedurende een langere periode
De mate van pijn weerspiegelt direct de ernst van de schade
Veel pijn is veel schade, weinig pijn, niet zo veel aan de hand
Pijn is niet gelijk aan schade
Pijn is geen betrouwbare graadmeter voor de toestand van het lichaam. Pijn is wél een betrouwbare graadmeter voor de toestand van het brein. Pijn kan blijven bestaan nadat weefsels zijn hersteld, door veranderingen in het zenuwstelsel
Het is niet voor altijd
Hersenen en ruggenmerg kunnen zich aanpassen op een manier die pijn in stand houdt
Het is een autonoom iets
Chronische pijn is een eigen aandoening waarin neuroplasticiteit een rol speelt
Niet solo maar een orkest
Pijn ontstaat uit samenspel van zenuwstelsel, afweer en psychologische processen
Nu
Nieuwe kijk

Wat dit voor een patiënt betekent
Aanhoudende pijn betekent niet dat iemand het zich inbeeldt of dat er altijd (nog) weefselschade is.
Vaak wijst het erop dat het zenuwstelsel en afweerreacties zijn veranderd op manieren die men kan begrijpen, beïnvloeden en reguleren — en die in veel gevallen kunnen verbeteren met passende, multidisciplinaire zorg.
Dit inzicht opent de deur naar behandelopties die zich richten op hoe het zenuwstelsel pijn verwerkt —
niet alleen op de plek waar het ooit begon.
Vijf belangrijke inzichten
Inzichten die ons begrip van chronische pijn ingrijpend hebben veranderd
1. Centrale sensitisatie
De ‘volumeknop' van het zenuwstelsel gaat omhoog
Wat het is
Centrale sensitisatie beschrijft hoe ruggenmerg en brein prikkelbaarder worden en pijnsignalen versterken.
Zie het als een volumeknop die te hoog staat: normale prikkels kunnen pijnlijk gaan voelen, en pijnlijke prikkels worden veel heftiger ervaren.
Door die verhoogde gevoeligheid reageren zenuwcellen in het centrale zenuwstelsel sterker op normale of zelfs milde input.
Dat kan leiden tot hyperalgesie (meer pijn bij pijnlijke prikkels) en allodynie (pijn bij normaal niet-pijnlijke prikkels).
Hoe het ontstaat
Herhaalde of heftige input vanuit (geïrriteerde) zenuwen in de periferie kan moleculaire veranderingen op gang brengen
in ruggenmerg en brein. Bijvoorbeeld:
Activatie van bepaalde receptoren (zoals NMDA-receptoren)
Veranderingen in ionkanalen die zenuwsignalen sturen
Versterking van synaptische verbindingen in pijnbanen
Minder effectieve, natuurlijke pijnremming
Waarom centrale sensitisatie een ‘onlogische’ chronische pijn klacht kan verklaren:
Pijn “niet in verhouding”: centrale sensitisatie verklaart waarom pijn heftiger kan zijn dan je verwacht op basis van weefselschade
Pijn die uitwaaiert: waarom pijn zich kan uitbreiden naar andere gebieden (‘Als ik hier druk, doet het daar pijn’)
Behandelresistentie: waarom alleen focussen op de oorspronkelijke plek vaak tekortschiet.
Richting voor behandeling
Behandeling kan zich nu richten op het dempen van die centrale prikkelbaarheid — met bepaalde medicatie,
neuromodulatie (oa TENS), geleidelijk opbouwen van activiteit en therapieën die de natuurlijke pijnremming helpen herstellen Dit in plaats van alleen te focussen op ‘repareren’ van perifere weefsels.
2. Neuroplasticiteit in het brein
Het brein kan veranderen bij chronische pijn
Hersenonderzoek met beeldvorming laat zien dat chronische pijn samenhangt met langdurige veranderingen in structuur en functie.
Dat zijn niet per se tekenen van ‘beschadiging’, maar van aanpassing — aanpassingen die ook pijn kunnen onderhouden.
We zien:
- Veranderd volume van grijze stof in pijn-gerelateerde gebieden
- Veranderingen in de prefrontale cortex en limbische gebieden
- Herorganisatie van de hersenschors in gebieden die gevoel verwerken
Chronische pijn kan de communicatie tussen hersennetwerken veranderen:
Default mode network: beïnvloedt zelfbewustzijn en “afdwalen” van gedachten
Salience network: beïnvloedt wat het brein als belangrijk markeert, inclusief pijnsignalen
Sensorimotor netwerk: beïnvloedt bewegen en verwerking van gevoel

🧩 Waarom dit vaak herkenbaar is
Deze veranderingen helpen verklaren waarom chronische pijn vaak samengaat met:
-Slaapproblemen
-Aanhoudende vermoeidheid
-Angst en somberheid/depressie
-Concentratie- en geheugenproblemen
🌱Perspectief op verandering.
Omdat dit ‘plastische’ veranderingen zijn (het brein heeft zich aangepast), kunnen ze mogelijk ook beïnvloed worden.
Denk aan revalidatie, cognitieve therapieën, mindfulness en neuromodulatie — allemaal gericht op het hertrainen van netwerken.
Het verschilt per persoon, maar het vermogen van het brein om te veranderen werkt twee kanten op.
3. Neuro-inflammatie en gliacellen
Afweercellen in het zenuwstelsel kunnen overactief worden
De ontdekking
Toen ik studeerde waren die cellen er . Glia. Zomaar. Ter ondersteuning? We/ze wisten het niet. Onderzoekers ontdekten ondertussen dat niet-neuronale cellen in het zenuwstelsel — microglia en astrocyten — wel degelijk een functie hebben: na een blessure of prikkel kunnen ze activeren en stoffen kunnen afgeven die centrale sensitisatie versterken en onderhouden.
Deze neuro-inflammatoire respons wordt gezien als een belangrijke schakel tussen een prikkel in de periferie en blijvende veranderingen in de pijnverwerking in ruggenmerg en brein.
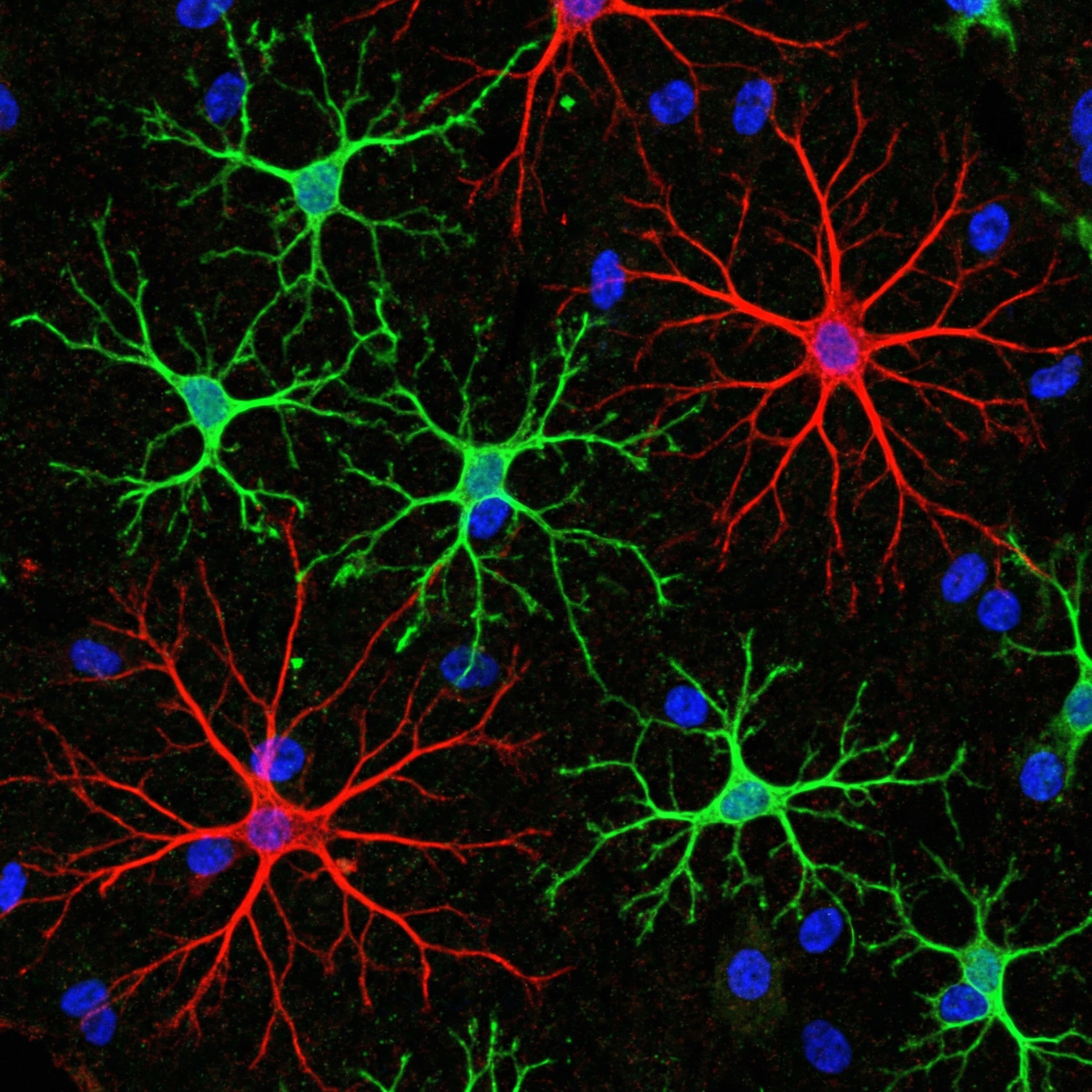
Microglia en astrocyten kunnen hun gedrag veranderen na zenuwirritatie of -letsel:
-Ze geven cytokinen en chemokinen af (ontstekingssignalen)
-Die signalen verhogen de prikkelbaarheid van zenuwcellen
-Ze beïnvloeden hoe synapsen (zenuwverbindingen) werken
-Het proces kan zich uitbreiden in netwerken in ruggenmerg en brein
Dit kan een zichzelf versterkende en in stand houdende cyclus worden:
1 Een prikkel activeert gliacellen
2 Gliacellen geven ontstekingssignalen af
3 Signalen verhogen zenuwgevoeligheid
4 Meer zenuwactiviteit activeert glia nog verder
Gliacellen kunnen zowel beschermend als problematisch zijn. Afhankelijk van de context kunnen ze herstel ondersteunen
of juist ontsteking en prikkelbaarheid in stand houden. Dat biedt kansen: we willen het helpende deel versterken
en het schadelijke deel dempen.
Betekenis voor behandeling
Het beïnvloeden van glia-signalen en centrale ontstekingsroutes is een belangrijk onderzoeks- en behandelgebied geworden.
Nieuwe benaderingen proberen te voorkomen dat pijn chronisch wordt en willen versterking van pijn verminderen door overactieve glia te kalmeren.
4. Bijdrage van het immuunsysteem
Chronische pijn is een neuro-immuun aandoening
👓 De nieuwe kijk
Aangeboren en verworven afweercellen kunnen samenwerken met perifere zenuwen en centrale glia en zo het risico op pijn,
het blijven bestaan ervan en herstel beïnvloeden. Onderzoek beschrijft chronische pijn steeds vaker als een
neuro-immuun aandoening — niet alleen een ‘zenuwprobleem’.
🦠 Perifere afweerprocessen
Na een blessure of infectie kunnen immuuncellen in weefsels en zenuwknopen (ganglia) stoffen afgeven :
Macrofagen: geven ontstekingssignalen af die pijnzenuwen gevoeliger maken
Neutrofielen: vroege responders die blijvende veranderingen kunnen uitlokken
Mestcellen: geven histamine en andere pijnbevorderende stoffen af
🧬 Rol van adaptieve afweer
B- en T-lymfocyten (adaptieve afweercellen) kunnen onverwachte rollen spelen:
*Kunnen bijdragen aan het ontstaan van sommige chronische pijnbeelden
*Kunnen pijn in bepaalde aandoeningen onderhouden
*Kunnen ook bijdragen aan herstel (afhankelijk van context)
🔗 Koppeling tussen CZS en afweer
Activatie van de afweer blijft niet altijd op één plek. Het kan:
- Centrale gliacellen in ruggemerg en brein beïnvloeden
- Cytokineniveaus in het centrale zenuwstelsel verhogen
- Neuro-inflammatie veroorzaken die de centrale sensitisatie in stand houdt
- Bijdragen aan hersenveranderingen die pijn onderhouden
🧪 Biomarkers en behandeling
In patiëntstudies zijn systemische ontstekingsmarkers in verband gebracht met pijnervaring.
Immunomodulerende benaderingen — behandelingen die de afweeractiviteit beïnvloeden — zijn een opkomend spoor in pijnonderzoek, met perspectief op gerichtere therapieën.
5. Biopsychosociale factoren
Stress, trauma en levenservaringen kleuren pijn
De samenhang
Psychologische stress, tegenslag vroeg in het leven en sociale factoren kunnen het zenuwstelsel en afweersysteem beïnvloeden en daarmee het risico vergroten dat acute pijn chronisch wordt.
Moderne modellen verbinden deze biopsychosociale factoren
met de ‘chronificatie’ van pijn: biologie, gedrag en omgeving werken samen en bepalen het verloop.
Biologisch
• Genetica
• Veranderingen in het zenuwstelsel
• Afweerreacties
• Hormonen
Psychologisch
• Stress en trauma
• Stemming en angst
• Opvattingen over pijn
• Coping / omgaan met pijn
Sociaal
• Sociaal support
• Werkomgeving
• Culturele factoren
• Toegang tot zorg
De biologie van stress
Chronische stress en traumatische ervaringen kunnen meerdere pijngerelateerde systemen beïnvloeden
Dalende pijnremming
Stress kan de natuurlijke pijnremmende banen vanuit de hersenen verzwakken, waardoor je gevoeliger wordt voor pijnsignalen.
Afweer
Chronische stress kan ontstekingsmarkers verhogen en afweerreacties activeren die bijdragen aan pijn.
Neuroplasticiteit
Stresshormonen kunnen hersenaanpassingen versterken die chronische pijn in stand houden, waardoor het zenuwstelsel ‘toeschietelijker’ wordt voor aanhoudende pijn.
Emotionele verwerking
Trauma en stress beïnvloeden limbische hersengebieden die betrokken zijn bij de emotionele kant van pijn, wat het lijden kan vergroten.
Psychosociale Versterking
Verschillende factoren kunnen samen met centrale sensitisatie pijn en beperkingen onderhouden:
- Aandachtsfocus: voortdurend “checken” van pijn kan het versterken
- Bewegingsangst: activiteit vermijden kan pijn en beperkingen verergeren
- Stemmingsklachten: somberheid en angst kunnen pijnbeleving versterken, soms kip en ei
- Sociale isolatie: gebrek aan steun verergert de situatie en outcome
Wat dit betekent voor zorg
Effectieve zorg bij chronische pijn is bij voorkeur multidisciplinair: aandacht voor lichamelijke, emotionele en sociale factoren,
niet alleen voor (mogelijke) weefselschade. Daarom combineren goede pijnprogramma’s vaak fysiotherapie, psychologische ondersteuning, sociale ondersteuning en medische behandeling.
Vragen die patienten vaak stellen
FAQs
Dit is één van de belangrijkste inzichten van de afgelopen 20 jaar. Nadat het oorspronkelijke letsel is hersteld, kunnen veranderingen in je zenuwstelsel — centrale sensitisatie, neuroplasticiteit, neuro-inflammatie en activatie van het immuunsysteem — blijven bestaan. Je systeem heeft als het ware ‘geleerd’ om
pijnsignalen te blijven geven, ook zonder voortdurende weefselschade. Daarom zien we chronische pijn steeds meer als een aandoening van het systeem zelf, en niet alleen als een symptoom van letsel.
Standaard beeldvorming (röntgen, MRI, CT) laat vooral structurele veranderingen in weefsels zien — botbreuken, gescheurde banden, of een hernia. Maar chronische pijn gaat vaak over functionele veranderingen: hoe je zenuwstelsel signalen verwerkt, niet per se over voortdurende weefselschade.
Gespecialiseerde hersenbeeldvorming laat zien dat mensen met chronische pijn meetbare veranderingen kunnen hebben in structuur, verbindingen en functie van het brein — maar dat is niet zichtbaar op routinematige scans. Een ‘normale’ scan sluit echte pijn niet uit; het zegt alleen dat de pijn waarschijnlijk niet komt door voortdurende weefselschade.
Nee. Chronische pijn is biopsychosociaal: biologische, psychologische én sociale factoren spelen samen. Dat zijn allemaal echte, meetbare processen.
De biologische veranderingen (centrale sensitisatie, neuro-inflammatie, immuunactivatie) zijn fysiek en meetbaar
Psychologische factoren (stress, trauma) beïnvloeden deze biologische processen door te eten mechanismes: stress hormonen, veranderde signaaldoorgifte in het brein, en immuun systeem signalen.
Dat er psychologische componenten meespelen betekent niet dat het ‘ingebeeld’ is. Het betekent dat je brein en emoties onderdeel zijn van het pijnsysteem —
en dat is logisch, want je brein verwerkt alle pijnsignalen.
Het idee van ‘genezen’ is bij chronische pijn ingewikkeld, er is zeker goed perspectief op verbetering. Doordat zoveel factoren invloed hebben, is het koffiedik kijken qua prognose.
Omdat chronische pijn samenhangt met neuroplastische veranderingen (aanpassing van het zenuwstelsel), kunnen die veranderingen vaak beïnvloed worden, en weer ’terug’ aangepast.
Veel mensen boeken duidelijke vooruitgang met:
• Behandelingen die centrale sensitisatie verminderen
• Therapieën die pijnverwerking in het brein kunnen beïnvloeden
• Benaderingen die neuro-inflammatie dempen
• Psychologische interventies die zich richten op stress en trauma (EMDR, PRT, CBT)
• Leefstijlveranderingen die het zenuwstelsel ondersteunen
Niet iedereen wordt volledig pijnvrij, maar veel mensen kunnen pijnintensiteit verminderen, beter functioneren en hun kwaliteit van leven sterk verbeteren.
De sleutel is vaak een brede, multidisciplinaire aanpak die alle onderhoudende factoren meeneemt.
Medische opleidingen en de dagelijkse praktijk lopen soms achter op onderzoek. Veel van deze inzichten zijn in de afgelopen 10–20 jaar snel ontwikkeld.
Het vertalen naar routinezorg vraagt tijd, training en veranderingen in het zorgsysteem.
Daarnaast is het in een kort consult lastig om complexe mechanismen rustig uit te leggen. Veel artsen kennen deze concepten wel, ze hebben niet altijd de ruimte gehad om er zo uitgebreid doorheen te gaan, dat ze het in vijf minuten kunnen uitleggen.
Als je behandelingen wilt die bij deze inzichten passen, kan ik je verwijzen naar een multidisciplinair pijnteam of pijnspecialist die met deze moderne kijk op chronische pijn werkt.
Voor patiënten met chronische pijn: het Pijnkompas zelfwerkboek
Naast professionele begeleiding kan dit gratis werkboek helpen bij zelfmanagement:
"Dit werkboek helpt je om een actieve rol te nemen in het omgaan met chronische pijn. Je vindt er wetenschappelijk onderbouwde informatie over hoe pijn werkt, gecombineerd met praktische oefeningen die je in je eigen tempo kunt doen. Het werkboek bestaat uit 11 hoofdstukken die je stap voor stap meenemen langs verschillende aspecten van omgaan met pijn: van begrijpen hoe pijn werkt tot concrete strategieën voor beweging, stress en dagelijkse activiteiten.
Je kunt het gebruiken als zelfstandige hulpbron of als aanvulling op een behandeling. Werk in je eigen tempo. Er moet niets."

Het werkboek is gratis beschikbaar voor iedereen met chronische pijn
Klik op de afbeelding voor download, zet niet gelijk je printer aan, het is 110 pagina’s
Bronnen:
Deze paginais gebaseerd op peer-reviewed onderzoek uit toonaangevende tijdschriften
Belangrijke publicaties:
Neumann, S., Sharma, A., & Maciaczyk, J. (2025).
Editorial: Insights into molecular and cellular mechanisms of chronic pain and neuroinflammation.
Frontiers in Molecular Neuroscience.
https://doi.org/10.3389/fnmol.2025.1679721
Sandkühler, J. (2017).
Neuroinflammation and Neuroplasticiteit in Pain.
Oxford Research Encyclopedia of Neuroscience.
https://doi.org/10.1093/ACREFORE/9780190264086.013.56
Ji, R. R., Nackley, A. G., Huh, Y., Terrando, N., & Maixner, W. (2018).
Neuroinflammation and Centrale sensitisatie in Chronic and Widespread Pain.
Anesthesiology, 129(2), 343-366.
https://doi.org/10.1097/ALN.0000000000002130
Varrassi, G., Leoni, M. L. G., Farì, G., et al. (2025).
Neuromodulatory Signaling in Chronic Pain Patients: A Narrative Review.
Cells, 14(17), 1320.
https://doi.org/10.3390/cells14171320
Rabbitts, J. A., & Palermo, T. M. (2020).
A Conceptual Model of Biopsychosocial Mechanisms of Transition from Acute to Chronic Postsurgical Pain in Children and Adolescents.
Journal of Pain Research, 13, 3071-3080.
https://doi.org/10.2147/JPR.S239320
Let op: Deze pagina vat bevindingen samen uit 284 peer-reviewed studies (2005–2025), gevonden via meerdere databanken waaronder PubMed, Google Scholar en SciSpace.
De inhoud volgt de huidige wetenschappelijke consensus over mechanismen bij chronische pijn.

